Metionina
Proprietà e caratteristiche della metionina
La metionina è un amminoacido con catena laterale apolare, essa è presente nelle proteine nella configurazione L.
Il suo nome IUPAC è acido 2(S)-ammino-4-metilmercaptobutanoico, ma è nota anche come L-omo-S-metil-cisteina o di acido 2-ammino-4-metilmercaptobutirrico e viene indicata con le sigle Met e M.
Essa contiene un atomo di zolfo; la sua pk1 (la costante di dissociazione acida del gruppo carbossilico) e la sua pk2 (la costante di dissociazione acida del gruppo amminico) sono rispettivamente pari a 2,13 e 9,28.
La metionina ha un pI (punto isoelettrico) di 5,74.
La sua formula bruta è C5H11NO2S, pertanto essa ha una massa molare di 149,21 g/mol.
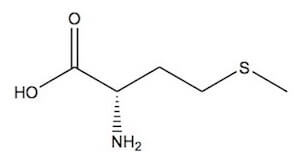
L-metionina.
La metionina si presenta come un solido cristallino biancastro, ha una solubilità in acqua pari a 48 g/L a 20 °C e la sua temperatura di fusione è 280 °C.
Proprietà della metionina
La metionina è un amminoacido essenziale, in quanto essa non può essere prodotta dall'organismo, quindi deve essere assunta con la dieta.
Le principali fonti alimentari di questo amminoacido sono: uova (in particolare l'albume), merluzzo, selvaggina, spirulina (alga), soia, latticini (latte, parmigiano, grana), storione, tacchino, pollo.
La metionina svolge diverse funzioni all'interno dell'organismo: essa si rivela un efficiente scavenger delle molecole ossidanti (ha, quindi, un alto potere antiossidante); è un chelante perché lega i metalli pesanti, come cadmio, piombo e mercurio, tossici per l'organismo a determinate concentrazioni, e ne facilita l'escrezione; è importante nella sintesi della colina, una biomolecola precursore di diverse molecole con funzioni nell'organismo; è fondamentale anche per mantenere i livelli di folato (o vitamina B9 o folacina), poiché una carenza di questo amminoacido causa anche una carenza di folato.
Essa è un intermedio nelle reazioni di transmetilazione, fungendo come maggior donatore di gruppi metile in vivo, tra cui i gruppi metilici per gli intermedi nella sintesi di DNA ed RNA.
Essa, inoltre, è essenziale per l'assorbimento, il trasporto e la biodisponibilità di selenio e zinco, che sono necessari all'organismo in quantità ridotte.
La metionina svolge anche la funzione di regolatore negativo dell'istamina, facilitandone l'escrezione.
Oltre a tutte queste funzioni, l'amminoacido è un importante costituente della pelle e dei tessuti, in particolare delle strutture cartilaginee, specialmente elastina, collagene, proteoglicani e glicosaminoglicani, delle proteine e degli enzimi presenti nei tessuti e dei peptidi noti come encefaline ed endorfine, che hanno funzione analgesica (o antidolorifica).
La metionina è coinvolta in una varietà di percorsi biochimici.
Molte cellule possono usare l'omocisteina come sostituto della metionina; comunque ci sono cellule metionina-dipendenti che non possono usare l'omocisteina in luogo della metionina.
I livelli di metionina influenzano la quantità di composti contenenti zolfo come il glutatione.
Quando i composti tossici sono presenti nell'organismo in grandi quantità, è necessario un maggiore apporto di metionina, che fornendo zolfo, migliora il tono e la flessibilità della pelle e dei capelli e la forza delle unghie.
La metionina, quindi, protegge le cellule dall'ossidazione.
Inoltre, essa agisce come agente lipotropico e inibisce l'accumulo di grassi nel fegato; essa contribuisce alla sintesi di numerosi composti fungendo da donatore di gruppi metilici; è importante anche per la sintesi di alcuni neurotrasmettitori, quali la dopamina, la noradrenalina, l'adrenalina e, soprattutto, la serotonina. La metionina è richiesta anche per la crescita e il riparo tissutale.
In genere, è necessaria una quantità di metionina giornaliera che varia dagli 800 ai 3000 mg.
Come per tutti gli amminoacidi, l'assorbimento della metionina ha luogo lungo l'intero intestino piccolo.
Un eccesso di amminoacidi, in genere, sovraccarica il fegato e i reni. Nel primo organo si forma l'ammoniaca.
Quando gli amminoacidi sono presenti in concentrazioni elevate, questo può determinare una scarsa digestione e un peggioramento della funzione renale.
Un forte eccesso di metionina può essere tossico. La dose che può causare tossicità negli adulti è intorno ai 350 mg/kg o circa 25 grammi giornalieri per una persona media.
Sintomi di tossicità possono includere iperattività, perdita di appetito, riduzione della crescita, atassia (mancanza di coordinazione dei movimenti muscolari volontari), emosiderosi (patologia dovuta a un eccesso di ferro) ed ematocrito molto basso.
Il derivato acetilato, la N-acetilmetionina, è meno tossico del precursore.
Dosi elevate aumentano l'escrezione urinaria di calcio e possono causare allucinazioni a dosaggi molto alti.
Comunque, dosi di 13 grammi al giorno sono ben tollerate con rare risposte avverse idiosincratiche.
L'omocisteina, che si forma per demetilazione della metionina, si accumula in caso di deficienza di vitamina B6.
Individui con elevati livelli di omocisteina e colesterolo sono a rischio di malattie cardiovascolari molto più della norma.
Vegetariani e vegani sono ad alto rischio di carenza di metionina (comunque, le carenze sono possibili anche in caso non si segua una dieta vegetariana).
Le principali cause di deficienza di questo amminoacido includono una dieta non sufficiente, stress, infezioni, scarso assorbimento ed età.
Deficienze di singoli amminoacidi non sono molto comuni, tranne in caso di dieta scarsamente varia.
Le carenze di amminoacidi sembrano più comuni come risultato di una totale deficienza di proteine.
Pazienti con HIV che mostrano disfunzione epatica cronica hanno mostrato un ridotto metabolismo della metionina.
Sintomi causati da moderata carenza di metionina includono ritardo della crescita e bassi livelli di proteine fondamentali nel sangue, mentre deficienze più severe si manifestano con apatia, edema, letargia (stato di sonno patologico profondo che comporta rilassamento muscolare e perdita di sensibilità), danni epatici, perdita di muscoli e grasso, lesioni della pelle, debolezza e depigmentazione dei capelli.
La metionina è un metil-accettore per l'enzima 5-metiltetraidrofolato omocisteina metiltransferasi o (metionina-sintasi), che catalizza l'unica reazione che permette il riciclo di questa forma di folato.
Questa funzione di accettore di gruppi metile è importante anche per il catabolismo della betaina.
La metionina è richiesta anche per la sintesi di cisteina.
Essa è il precursore metabolico della cisteina solo per quanto riguarda l'atomo di zolfo, mentre lo scheletro carbonioso della cisteina è fornito dalla serina.
L'Organizzazione Mondiale della Sanità (OMS) raccomanda una quantità giornaliera di 13 mg/kg in adulti sani.
Questa quantità è raddoppiata in caso di nutrizione artificiale, in alcune malattie o in seguito a traumi.
In casi specifici di deficienza enzimatica genetica, prematurità o ridotta funzione del fegato, può verificarsi ipermetioninemia (eccesso di metionina nel sangue) che può portare a omocisteinemia.
Un supplemento di amminoacidi sulfurei, comunque, può essere considerato sicuro in quantità che superano di 2-3 volte la minima raccomandata.
L'utilizzo di integratori può causare diarrea o temporanea flatulenza.
Il ruolo della metionina come precursore dell'omocisteina è molto noto ed è grande fonte di preoccupazione.
In uno studio, è stata somministrata una dose di metionina di 0,1 g/kg, che ha portato all'aumento dei livelli plasmatici di omocisteina, che è un indice della suscettibilità di malattia cardiovascolare.
Comunque, una dose maggiore di 10 volte rispetto a quella raccomandata, ingerita per errore, ha portato alla morte.
Studi recenti hanno indicato che, per gli adulti, non ci sono conseguenze avverse per fluttuazioni moderate nell'apporto di metionina dalla dieta, ma un apporto 5 volte maggiore del normale ha causato un aumento dei livelli di omocisteina.
Questi effetti sono ridotti da supplementi delle vitamine B6 e B12 e dell'acido folico.
Nei bambini, invece, l'integrazione di metionina in dosi superiori da 2 fino a 5 volte il normale fabbisogno ha causato riduzione della crescita, ma non sono state osservate ulteriori conseguenze avverse a lungo termine.
Applicazioni della metionina
La metionina ha diverse potenziali applicazioni.
Essa può essere usata nella depressione istadelica (forma della patologia caratterizzata da elevati livelli di istamina, da cui trae il nome).
Questi pazienti sono stati trattati con successo utilizzando la metionina, che, come già detto, contribuisce a ridurre i livelli di istamina.
Un'altra patologia a livello del sistema nervoso caratterizzata da un eccesso di istamina, in cui la metionina fornisce risultati incoraggianti, è la schizofrenia, anche se la metionina è nota per esacerbare i sintomi psicopatologici in pazienti schizofrenici (ma non c'è prova di questi effetti in soggetti sani).
Infine, essa fornisce un ottimo contributo alla detossificazione dell'organismo operata del fegato, vista la sua funzione di donatore di zolfo, in particolare come precursore dell'antiossidante glutatione.
Comunque, oltre ad alcune indicazioni molto specifiche come l'avvelenamento da acetaminofene, l'utilità degli integratori di questo amminoacido non è stabilita con certezza.
Biochimica della metionina
La metionina è il precursore dell'amminoacido cisteina.
La metionina subisce reazione di transmetilazione ad opera dell'enzima metionina adenosil transferasi, che utilizza una molecola di ATP e porta alla formazione della L-omocisteina e dei sottoprodotti, 3 ioni fosfato (Pi) e S-adenosilmetionina (SAM).
Quest'ultima molecola è un importante cofattore, che dona gruppi metile in diverse reazioni catalizzate dagli enzimi metiltransferasi, coinvolti in diverse reazioni biosintetiche.
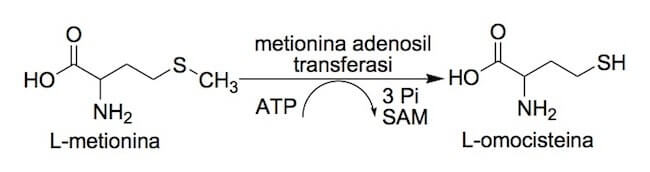
Formazione dell'omocisteina a partire dalla metionina.
La successiva reazione reversibile, la transolforazione, è catalizzata dall'enzima cistationina beta sintasi: l'omocisteina reagisce con la L-serina per formare la L-cistationina e una molecola d'acqua.
Infine, la cistationina entra nella reazione chimica catalizzata dalla cistationina gamma-liasi, che porta alla formazione della cisteina e dell'acido alfa-chetobutirrico.
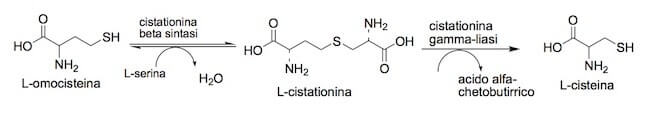
Sintesi della cisteina a partire dall'omocisteina.
La metionina può essere convertita in succinil-coenzima A (succinil-CoA), che entra nel ciclo di Krebs, un processo fondamentale per il metabolismo energetico dell'organismo ed è il precursore delle porfirine, come l'eme presente nell'emoglobina, la proteina che trasporta l'ossigeno alle cellule.
Dalla metionina si forma il propionil-coenzima (propionil-CoA), che viene poi trasformato, mediante un processo in tre tappe, in succinil-CoA.
L'acido alfa-chetobutirrico, derivante dalle reazioni viste in precedenza, viene trasformato in propionil-CoA nella reazione catalizzata dall'alfa-chetoacido deidrogenasi.
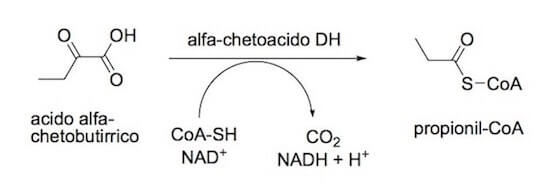
Formazione del propionil-CoA.
Durante la traduzione o sintesi proteica, l'amminoacido metionina è codificato dalla tripletta di nucleotidi ATG, che è il codone di inizio di tale processo.
Link correlati:
Proprietà e caratteristiche dell'inositolo
Che cosa sono le liasi?
Che cosa identifica il simbolo m?
Studia con noi