Temperatura o punto di fusione
Temperatura o punto di fusione: definizione e spiegazione
È noto che una sostanza può presentarsi in più stati di aggregazione (solido, liquido, vapore, ecc.), ciascuno dei quali ha un ben definito campo di stabilità. La fusione è il passaggio di una sostanza dallo stato solido allo stato liquido e la temperatura alla quale avviene è detta temperatura di fusione.
Per meglio comprendere quanto detto pendiamo in esame un blocco di ferro e supponiamo di riscaldarlo. Inizialmente la sua temperatura inizia a crescere fino a raggiungere una temperatura alla quale il blocco di ferro inizia a fondere, ovvero inizia a trasformarsi in un liquido. La temperatura alla quale avviene tale processo è detta temperatura di fusione.
In base a quanto appena detto risulta quindi che la fusione è il passaggio dallo stato solido allo stato liquido del ferro o più in generale di un corpo. Per ottenere la fusione di una sostanza occorre somministrare calore dall'esterno.
Come si vedrà più avanti, durante la fusione del ferro (o di qualsiasi altra sostanza, come ad esempio il ghiaccio) la temperatura rimane costante; il calore somministrato nel periodo della fusione si chiama calore latente di fusione.
Quindi ricorda che: la temperatura di fusione è la temperatura alla quale avviene la fusione di una sostanza; tale temperatura permane per tutto il tempo in cui si ha il passaggio da solido a liquido.
Influenza della pressione sulla temperatura di fusione
La temperatura di fusione dipende dalla pressione che agisce sul solido; questa influenza però non si rende sensibile che per grandi variazioni di pressione.
In generale, un aumento della pressione fa abbassare la temperatura di fusione in quelle sostanze che si contraggono passando dallo stato solido allo stato liquido (ghiaccio) e la fa innalzare in quelle sostanze che si dilatano nel passaggio medesimo.
In altre parole:
- se nella fusione la specie chimica aumenta di volume (∆V > 0), ad un aumento di pressione corrisponde a un aumento della temperatura di fusione, e ciò significa che la fusione avviene con più difficoltà: l'aumento di pressione ostacola la fusione;
- se nella fusione la specie chimica diminuisce di volume (∆V < 0), la temperatura di fusione diminuisce al crescere della pressione e quindi l'aumento di pressione favorisce la fusione. Questo caso, assai raro, si riscontra per H2O, Sb, Bi, Ga.
Quindi, per l'acqua che contrae il proprio volume passando dallo stato solido allo stato liquido, un aumento di pressione permette la fusione del ghiaccio a temperature inferiori a 0°C. La pressione necessaria per fondere il ghiaccio a -1°C è molto alta, pari a 133 atmosfere; un pattinatore di 70 kg che preme sul ghiaccio con una lamina di superficie pari a 0,5 cm2 raggiunge questa pressione.
Temperatura di fusione e curva di riscaldamento di una sostanza pura
Prendiamo in esame i fenomeni che si verificano durante il progressivo riscaldamento di un solido come ad esempio l'acqua. Un cubetto di ghiaccio viene posto in una adatta apparecchiatura che gli fornisce assai lentamente quantità note di calore e che ne registra la sua temperatura.
Si immagini di operare alla pressione atmosferica e di riportare su un diagramma le temperature del ghiaccio in funzione dei successivi tempi di riscaldamento; si ottiene un diagramma come quello illustrato nella figura seguente.
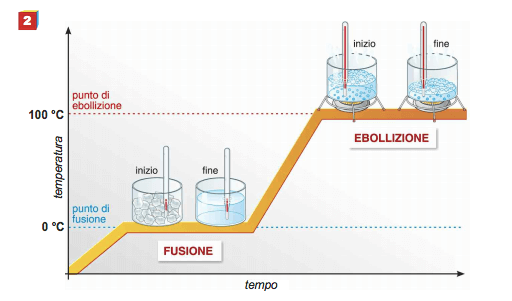
Curva di riscaldamento dell'acqua distillata: si nota che durante la fusione la temperatura rimane costante a 0°C. Tale temperatura è detta temperatura (o punto) di fusione.
Nel primo tratto della curva, che giunge sino alla temperatura di fusione, il calore fornito al solido fa aumentare la temperatura di questo dalla temperatura di inizio esperienza sino a 0°C; parallelamente aumenta l'energia cinetica (di vibrazione) delle particelle che lo costituiscono.
Nel secondo tratto della curva, quello relativo alla fusione (primo tratto orizzontale alla temperatura di 0°C), l'energia cinetica media delle particelle del solido raggiunge il valore necessario per provocare la rottura del reticolo, ed il solido comincia a fondere: 0°C è la temperatura di fusione del ghiaccio.
Fornendo ulteriormente calore al sistema solido/liquido non si ha aumento di temperatura poiché l'energia fornita al sistema è usata per rompere i legami reticolari del solido. Durante questa fase la temperatura rimane quindi costante sino a quando tutto il ghiaccio si è fuso.
Poiché la quantità di calore fornita al solido nel passaggio di stato solido → liquido non provoca aumento della temperatura del solido, ad essa è attribuito l'aggettivo latente. Si parla così di calore latente di fusione, che, se riferito ad una mole di solido che passa allo stato liquido, prende il nome di calore latente molare di fusione.
Una volta che tutto il solido si è fuso ed il sistema è costituito da solo liquido, continuando a fornire calore si ha di nuovo aumento dell'energia cinetica media delle particelle di liquido, e quindi della temperatura, fino all'ebollizione della sostanza.
Temperatura di fusione o punto di fusione di alcuni materiali
Riportiamo i valori delle temperature di fusione di alcune sostanze determinate alla pressione di 1 atm.
Temperatura di fusione dell'alluminio = 660,3°C
Temperatura di fusione dell'ossigeno (-218,4°C)
Temperatura di fusione dell'azoto (-210°C)
Temperatura di fusione dell'alcol etilico (-115°C)
Temperatura di fusione del mercurio (-38,8°C)
Temperatura di fusione dell'acqua (0°C)
Temperatura di fusione del sale da cucina (801°C)
Temperatura di fusione dell'oro (1065°C)
Link correlati:
Che cos'è la temperatura di ebollizione?
Quanto vale i calore latente dell'acqua?
Studia con noi