Benzene
Proprietà e caratteristiche del benzene
Il benzene è un composto organico con formula bruta C6H6. È il primo e il più importante termine della serie degli idrocarburi aromatici.
Fu scoperto nel 1825 dal chimico britannico M. Faraday, che lo isolò da un condensato oleoso depositatosi dal gas illuminante.
Fu ottenuto successivamente nel 1834 da E. Mitscherlich (che ne determinò la formula bruta e la massa molecolare) per distillazione su calce dell'acido benzoico:
C6H6COOH → C6H6 + CO2
Negli anni seguenti il chimico tedesco J. von Liebig gli diede il nome benzolo. Per evitare confusione con gli alcoli, la desinenza -olo fu successivamente modificata in -ene e l'attuale nome benzene, accettato anche dalla IUPAC, risulta il più corretto.
Il benzene è un liquido mobile, incolore, con temperatura di ebollizione di 80,1 °C e temperatura di fusione di 5,48 °C; in condizioni standard ha una densità di 0,8765 g/cm3 (è quindi più leggero dell'acqua).
È facilmente infiammabile e forma allo stato di vapore miscele esplosive con l'aria; è miscibile con i comuni solventi organici
Alla temperatura di 20°C ha una solubilità in acqua pari a 1,770 g/L e forma con questa un azeotropo (91,17% in peso di benzene, punto di ebollizione 69,25 °C); .
È una sostanza tossica e la prolungata permanenza in ambienti contenenti vapori di benzene produce nausea, senso di stanchezza e anche anemia; alte concentrazioni di benzene possono invece portare alla morte.
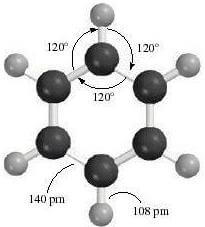
Struttura del benzene
Al riguardo si veda la seguente voce: struttura del benzene.
Produzione del benzene
Prima della seconda guerra mondiale la distillazione (cokizzazione) del carbon fossile costituiva l'unica fonte di benzene.
In questo processo il benzene viene estratto dal gas di cokeria, per adsorbimento su carbone attivo o per lavaggio con olio pesante (debenzolaggio).
Il prodotto grezzo ottenuto viene lavato con acido solforico e con alcali caustici per asportare le impurità costituite rispettivamente da prodotti basici e fenolici; viene in seguito rettificato per separarlo dagli omologhi, principalmente dal toluene.
Durante la seconda guerra mondiale l'aumentata richiesta di idrocarburi aromatici, particolarmente di toluene, impiegato nella preparazione del tritolo, diede l'impulso per la ricerca di nuove fonti di produzione.
Così, dal 1940 al 1948, sono stati messi a punto processi di aromatizzazione del petrolio, consistenti nel trasformare, mediante un complesso di reazioni di cracking, ciclizzazione e deidrogenazione, i componenti paraffinici e naftenici in idrocarburi aromatici.
Il processo base per ottenere aromatici, e quindi benzene, è il reforming catalitico, completato da una estrazione con solventi selettivi e dal successivo frazionamento per distillazione.
Un prodotto di reforming da benzine di prima distillazione contiene in media il 3,5% di benzene. Per aumentare le rese in benzene si può ricorrere ai processi di dealchilazione di aromatici superiori (per esempio toluene), per idrodealchilazione catalitica o termica.
Impieghi del benzene
Il benzene costituisce la materia prima per la preparazione, attraverso numerosi e importanti intermedi (clorobenzene, nitrobenzene, fenolo, anilina, etilbenzene, ecc.), di una vastissima gamma di coloranti, di resine sintetiche, di materie plastiche, di fibre tessili sintetiche, di farmaci e di numerosi altri composti (prodotti finiti).
Il benzene trova infine impiego anche nella produzione del polistirene.
Link correlati:
Quali sono le reazioni caratteristiche del benzene?
Per quale motivo il benzene non dà reazioni di addizione?
Calcolo della densità del benzene
Caratteristiche del bifenile
Proprietà e caratteristiche del difenilmetano
Proprietà e caratteristiche del fenantrene
Link correlati:
Proprietà e caratteristiche dell'anisolo
Che cos'è un arile?
Studia con noi