Toluene (toluolo)
Proprietà e caratteristiche del toluene
Il toluene, noto anche con il nome di metilbenzene o di toluolo, è un composto aromatico con formula bruta C7H8.
Presenta la seguente struttura:
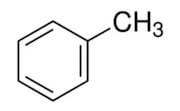
Ha massa molare di 92,14 g/mol, punto di fusione di -95°C, punto di ebollizione di 110,6°C.
La sua densità è pari a 0,81 g/cm3.
Il toluene è un composto insolubile in acqua e solubile in tutti i solventi organici; è facilmente infiammabile.
I suoi vapori sono tuttavia tossici, anche se meno di quelli del benzene.
Reazioni del toluene
Più facilmente del benzene il toluene può essere attaccato da reagenti elettrofili per dare reazioni di sostituzione elettrofila aromatica poiché contiene il gruppo metilico che è un sostituente attivante.
Reazioni come l'alogenazione possono essere condotte sia sul nucleo (in tal caso si opera in presenza di catalizzatori quali cloruro di alluminio o di ferro) sia sulla catena laterale (si opera in assenza di catalizzatori e in presenza di luce, e la reazione procede a stadi).
Le reazioni di sostituzione al metile avvengono infatti con un meccanismo radicalico analogo a quello degli alcani (al riguardo si veda: alogenazione degli alcani).
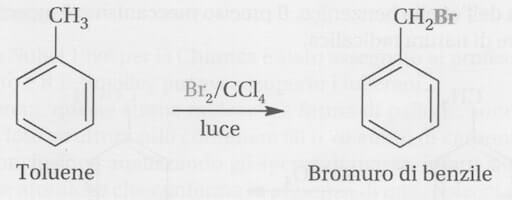
Sostituzione al metile del toluene
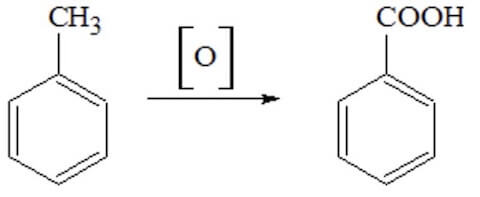
L'ossidazione all'aria in fase liquida del toluene ad acido benzoico si verifica a 150-175 °C e usa come catalizzatori i naftenati di cobalto e di manganese.
Preparazione del toluene
Per molto tempo il toluene è stato ottenuto esclusivamente dal catrame di carbone fossile.
Oggi è prodotto invece dalle frazioni del petrolio che contengono n-eptano per ciclizzazione e deidrogenazione catalitica del cicloalcano e anche per reforming e cracking di nafta.
Usi del toluene
Buona parte del toluene prodotto viene convertito in benzene e l'altra utilizzazione più rilevante è quella come solvente per le resine sintetiche, per gli agenti protettivi di superficie, per gli adesivi e prodotti collegati.
Come intermedio chimico l'uso principale tradizionale ancora importante, è per la preparazione dell'esplosivo TNT.
La produzione di toluene è stata stimolata dalla rapida crescita di importanza dei polimeri uretanici.
Il toluene era, ed è ancora, sottoposto a clorurazione a più stadi per ottenere cloruro di benzile, cloruro di benzale e benzotricloruro.
Questi composti possono essere idrolizzati ad alcol benzilico, o a benzaldeide o ad acido benzoico rispettivamente. Più di 36 milioni di chilogrammi di cloruro di benzile si producono annualmente, di cui il 60% porta a benzilftalato, un plastificante per mattonelle di vinile.
Studia con noi