Tirosina
Proprietà e caratteristiche della tirosina
La tirosina è un amminoacido con catena laterale polare, essa è presente nelle proteine nella configurazione L.
Il suo nome IUPAC è acido 2(S)-ammino-3-(4-idrossifenil)-propanoico, ma è nota anche come 3-(4-idrossifenil)-L-alanina e viene indicata con le sigle Tyr e Y.
La sua catena laterale è costituita dal gruppo p-idrossibenzile, che conferisce all'amminoacido una pkR di 10,46.
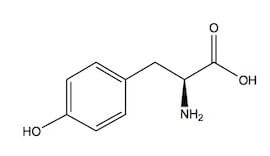
L-tirosina.
La tirosina ha una pk1 (la costante di dissociazione acida del gruppo carbossilico) e una pk2 (la costante di dissociazione acida del gruppo amminico) rispettivamente pari a 2,2 e 9,21.
Ha un pI (punto isoelettrico) di 5,64.
La sua formula bruta è C9H11NO3, pertanto essa ha una massa molare di 181,19 g/mol.
La tirosina si presenta come un solido cristallino incolore, ha una solubilità in acqua pari a 0,38 g/L a 20 °C e la sua temperatura di fusione è 342°C.
Funzioni biologiche della tirosina
La tirosina è un amminoacido non essenziale, poiché l'organismo umano può sintetizzarla.
Le principali fonti alimentari di questo amminoacido sono: spirulina (alga), stoccafisso, latticini (grana, gruviera, pecorino, latte, emmenthal, fontina, provolone), soia.
Il suo assorbimento avviene lungo l'intestino, in seguito alla digestione delle proteine che avviene nello stomaco.
La tirosina svolge numerose funzioni all'interno dell'organismo:
- è un importante costituente delle proteine;
- è il precursore dei neurotrasmettitori appartenenti alla classe delle catecolammine (DOPA, dopamina, noradrenalina, adrenalina), che, oltre a regolare le principali funzioni fisiologiche, sono coinvolte nella risposta allo stress, nelle funzioni intellettive e nell'umore;
- è un componente importante nella sintesi degli ormoni tiroidei tiroxina e triiodotironina, che regolano diverse funzioni metaboliche, tra cui il metabolismo degli zuccheri e dei grassi e la termogenesi, e regolano la funzione cardiovascolare;
- è necessaria per la formazione della melanina, il pigmento bruno che ha la funzione di proteggere le cellule dagli effetti dei raggi ultravioletti;
- è il precursore della colecistochinina, il neurotrasmettitore che, nel sistema nervoso centrale, regola il senso di sazietà;
- è coinvolta nelle trasduzione del segnale: la fosforilazione o la solfatazione dei residui di tirosina presenti nelle proteine regola la funzione di queste ultime, attivandole o inibendole a seconda dei casi.
La carenza di tirosina può verificarsi in alcune situazioni:
- dieta povera di proteine;
- acloridria o ipocloridria: soggetti affetti da queste condizioni producono scarse quantità di acido cloridrico nello stomaco, non digeriscono bene le proteine e quindi si ha un assorbimento ridotto o nullo di amminoacidi;
- fenilchetonuria: pazienti con questa patologia genetica hanno un deficit dell'enzima che converte la fenilalanina in tirosina e hanno quindi livelli di fenilalanina molto elevati;
- insufficienza renale terminale (ESRD): soggetti affetti da questa patologia presentano una scarsa sintesi di tirosina a partire dalla fenilalanina.
La tirosina può divenire condizionatamente essenziale, in condizioni o patologie in cui l'omeostasi dipende fortemente dalla tirosina.
Possono insorgere vari problemi in seguito a scarsi livelli di tirosina nell'organismo, a causa del suo coinvolgimento in numerosi processi metabolici.
I sintomi da carenza di tirosina includono:
- ipotiroidismo;
- ipotensione;
- abbassamento della temperatura corporea;
- depressione;
- disturbi emozionali e psicologici;
- aumento dell'appetito.
Gli integratori a base di tirosina, in genere, non presentano una particolare tossicità, quindi sono prodotti abbastanza sicuri.
Comunque, livelli di tirosina eccessivamente elevati possono portare a diversi sintomi:
- diarrea;
- nausea;
- vomito;
- mal di testa;
- nervosismo;
- lesioni oculari;
- scarso appetito.
Applicazioni cliniche della tirosina
Ci sono diversi studi riguardanti le applicazioni cliniche della tirosina.
Essa si è rivelata utile in caso di:
- dipendenza da cocaina: l'euforia data da questa sostanza d'abuso dipende dall'attivazione dopaminergica, che svuota le riserve di dopamina nel cervello e crea la dipendenza; la tirosina aiuta l'organismo a sintetizzare più dopamina, riducendo il bisogno di cocaina;
- depressione: dato che la tirosina è il precursore di dopamina e noradrenalina, è stata usata con un certo successo nel trattamento della depressione e si è visto che l'integrazione dell'amminoacido possa essere utile anche nell'alleviare la depressione che accompagna il morbo di Parkinson e la malattia di Alzheimer;
- miopatia nemalinica: secondo un recente studio, dosaggi di tirosina tra i 250 e i 3000 mg in pazienti con questa patologia si sono rivelati efficaci nel migliorare il livello di attività e la performance nell'esercizio fisico senza reazioni avverse;
- fenilchetonuria: questa patologia è caratterizzata dal deficit dell'enzima necessario alla sintesi di tirosina, quindi integratori dell'amminoacido sono utili per supportare la sintesi degli ormoni e dei neurotrasmettitori che dipendono dalla tirosina.
Biochimica della tirosina
La tirosina è sintetizzata nell'organismo a partire dall'amminoacido fenilalanina; si forma per reazione di idrossilazione della fenilalanina in un processo catalizzato dall'enzima fenilalanina idrossilasi.
L'amminoacido reagisce, in maniera reversibile, con l'ossigeno e la tetraidrobiopterina formando i prodotti idrossilati.
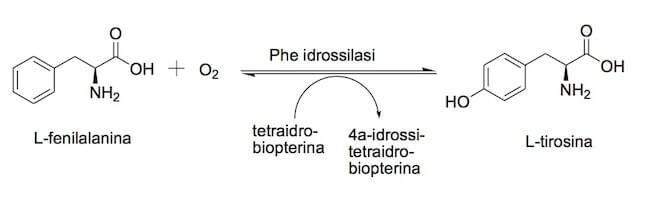
Reazione catalizzata dalla fenilalanina idrossilasi.
La tirosina, come già detto, è il precursore dei neurotrasmettitori DOPA, dopamina, noradrenalina e adrenalina.

La tirosina è considerata un amminoacido sia glucogenico sia chetogenico.
Infatti, essa può essere convertita in fumarato, che, nel ciclo di Krebs, viene convertito in ossalacetato, uno degli intermedi della gluconeogenesi, la serie di tappe biochimiche necessarie alla sintesi del glucosio (glucogenico).
Inoltre, la tirosina può essere convertita in acetoacetil-coenzima A, precursore per la sintesi dei corpi chetonici (chetogenico).
Durante la traduzione o sintesi proteica, l'amminoacido tirosina è codificato dalle triplette di nucleotidi TAT e TAC.
Studia con noi