Elettrone
Elettrone: caratteristiche e proprietà
In questa lezione vedremo che cos'è l'elettrone e quali sono le sue principali proprietà fisiche.
Vedremo a quale illustre scienziato si deve la scoperta dell'elettrone e quali esperimenti permisero l'identificazione di questa particella.
Studieremo infine due importanti proprietà dell'elettrone: il numero quantico di spin e il momento magnetico.
Che cos'è l'elettrone?
L'elettrone (rappresentato solitamente con il simbolo e−) è una particella elementare che è la componente a carica negativa della materia ordinaria; è la particella più leggera che sia dotata di carica. Viene classificato come fermione in quanto obbedisce alla statistica di Fermi-Dirac.
Secondo tutte le prove sperimentali svolte, l'elettrone è una particella stabile.
Insieme a protoni (carichi positivamente) e ai neutroni (neutro) costituisce la materia ordinaria e quindi la struttura dell'atomo.
Gli elettroni di un atomo, numericamente uguali al numero di protoni, si muovono attorno a un nucleo composto (in uno schema molto semplificato) da protoni (p+) e neutroni (n0); nel nucleo è quasi del tutto concentrata la massa dell'atomo.
Il volume di un atomo è quasi del tutto occupato dalla nuvola elettronica distribuita attorno al nucleo; quest'ultimo occupa infatti solo una frazione piccolissima (la 10-13-esima parte) dell'intero volume dell'atomo.
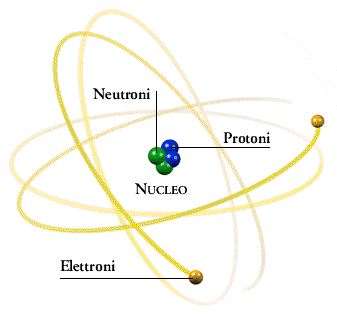
In un modello molto semplificato, l'atomo è costituito da un nucleo carico positivamente e da elettroni che ruotano attorno ad esso.
L'elettrone ha una massa a riposo di 9,1 · 10-31 kg, che corrisponde a 1/1836 volte la massa del protone o del neutrone, e una carica elettrica di -1,6 · 10-19 C (coulomb). Tale particella, alla quale per convenzione è stata attribuito il valore di carica elettrica -1, viene identificata con il simbolo e−.
Pertanto l'elettrone è una particella subatomica con carica elettrica negativa (-1) che si ritiene essere una particella elementare.
Scoperta dell'elettrone
Gli elettroni furono scoperti da J. J. Thomson nel 1897 nei processi di produzione dei raggi catodici, l'elettrone fu la prima particella elementare a essere identificata.
Nei suoi esperimenti Thomson utilizzò un tubo di Crookes; si tratta di un tubo di vetro resistente che viene mantenuto sotto vuoto spinto, alle estremità del quale sono applicati due elettrodi collegati rispettivamente con il polo positivo (anodo) e con il polo negativo (catodo) di un generatore di corrente.
Quando la differenza tra gli elettrodi raggiunge un valore elevato (10000 volt) e la pressione interna un valore bassissimo, si osserva l'emissione di raggi luminosi che, partendo dal catodo e propagandosi in linea retta, si dirigono verso l'anodo provocando sul vetro una tenue luminosità.
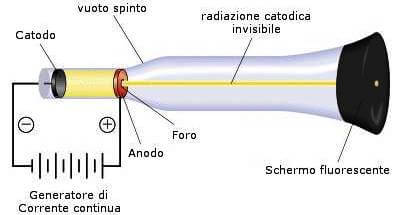
Tale fenomeno fu messo in relazione con possibili radiazioni che potevano essere prodotte dal catodo e che furono chiamate raggi catodici.
Oggi sappiamo che si tratta di elettroni che si muovono dal catodo verso l'anodo rendendo la parete che colpiscono fluorescente.
Successivi studi dimostrarono che tali raggi si propagano in linea retta dal polo negativo al polo positivo. Infatti i raggi proiettavono sulla parete l'ombra di un oggetto frapposto nel loro cammino:
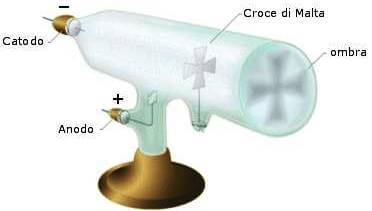
Finalmente, nel 1895, il fisico francese J. B. Perrin osservò che un elettroscopio colpito da radiazioni catodiche si elettrizzava negativamente.
Dimostrò in questo modo che i raggi catodici (ovvero gli elettroni) erano dotati di carica negativa.
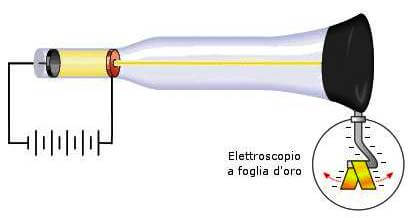
Successivi esperimenti dimostrarono che i raggi catodici erano dotati anche di una certa massa; infatti i raggi catodici erano in grado di fare ruotare un mulinello interposto nel loro cammino.

La carica elettrica dell'elettrone fu determinata per la prima volta nel 1911 dal fisico statunitense Robert A. Millikan (1868-1953) con un esperimento noto con il nome di esperimento di Millikan.
Il processo che si ha quando un atomo o una molecola acquistano un elettrone libero è detto cattura elettronica.
Carica dell'elettrone
Come si è detto in precedenza, la carica e dell'elettrone è 1,6·10-19 C. All'elettrone si assegna convenzionalmente una carica negativa, mentre al protone si assegna una carica positiva uguale, in valore assoluto, a quella dell'elettrone.
La misura diretta più precisa della carica dell'elettrone venne effettuata nel 1909 da R. A. Millikan per mezzo di un'esperiento atto a determinare il valore delle cariche distribuite su goccioline d'olio in aria equilibrando con un opportuno campo elettrico il peso delle goccioline stesse.
Il peso delle goccioline viene stabilito misurando la velocità di caduta libera nell'aria e inserendo tale valore nella formula della legge di Stokes, che permette di calcolare, per una sferetta che si muove lentamente, la resistenza che il mezzo viscoso esplica su essa. Si trova così che le cariche misurate sono multipli interi di e.
Per un ulteriore approfondimento si veda: esperimento di Millikan.
Spin dell'elettrone
Ogni particella elementare possiede una quantità di moto angolare intrinseca detta spin; lo spin dell'elettrone (che è uno dei quattro numeri quantici) è ½ħ, essendo ħ la costante di Planck (h) divisa per 2π.
L'elettrone però possiede due versi di rotazione attorno al proprio asse: l'uno destrorso (da sinistra verso destra) e l'altro sinistrorso (da destra a sinistra) indicati di solito con i termini rispettivamente di "spin su" (↑) e "spin giù" (↓); un elettrone può pertanto avere due stati di spin +½ħ e -½ħ.
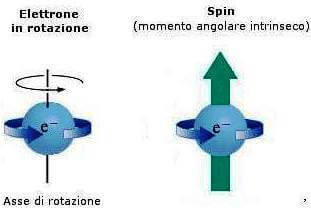
Lo spin dell'elettrone è dovuto al suo momento angolare intrinseco.
Momento magnetico dell'elettrone
L'elettrone rivela proprietà magnetiche dovute ai movimenti di rivoluzione attorno al nucleo e di rotazione (spin) attorno al proprio asse.
Il momento magnetico dell'elettrone, in base all'equazione di Dirac, è:
μD = (e·h) / (2·me)
Il momento magnetico effettivo μ differisce da μD di una piccola quantità (momento magnetico anomalo) dovuta alle correzioni radiative:
μ = 1,0011 · μD
Questo valore teorico, calcolato usando la teoria quantistica dei campi rinormalizzata, è in buon accordo con il valore sperimentale.
Link correlati:
Quesito (con soluzione) sull'elettroscopio
Come si realizza l'elettrizzazione per strofinio?
Chi è stato l'inventore del telefono?
Che cos'è il muone?
Che cos'è l'effetto termoionico?
Che cos'è la meccanica razionale?
Studia con noi