Enzimi digestivi
Che cosa sono gli enzimi digestivi?
Gli enzimi digestivi sono una classe di proteine che catalizzano una serie di reazioni necessarie per il completamento del processo di digestione. L'azione degli enzimi digestivi consente di scomporre le grandi macromolecole organiche in molecole più piccole, le quali sono in grado di attraversare la barriera intestinale ed essere così trasportate dai fluidi corporei.
Attraverso il sangue, le molecole più piccole riescono quindi a raggiungere tutti i distretti corporei ed essere assorbite dalle cellule per essere poi utilizzate per tutti i processi metabolici.
Gli enzimi digestivi sono tutti altamente selettivi per il tipo di substrato che sono in grado di attaccare e si dividono in varie categorie. Ogni categoria rispecchia il tipo di molecola per cui gli enzimi sono specializzati, ma tutti agiscono catalizzando una reazione di idrolisi che rompe il legame che tiene uniti due residui, aggiungendo un gruppo OH− ad uno dei due residui ed uno ione H+ all'altro.
In base al tipo di molecola che sono in grado di idrolizzare, distinguiamo i seguenti gruppi di enzimi digestivi:
- Proteasi: catalizzano la digestione delle proteine
- Carboidrasi: operano l'idrolisi dei carboidrati
- Lipasi: permettono la digestione delle molecole lipidiche
A questi tre gruppi principali di enzimi digestivi, fondamentali per il processo nutrizionale dell'organismo, si uniscono altri gruppi di minore importanza e non strettamente indispensabili.
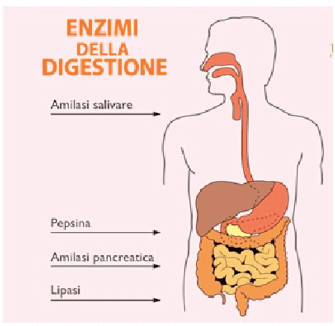
Figura 1: Alcuni dei principali enzimi digestivi.
Proteasi
Le proteasi agiscono attraverso l'idrolisi dei legami peptidici scomponendo oligopeptidi e polipeptidi in singoli amminoacidi.
Si dividono in due categorie: esoproteasi ed endoproteasi. Le endoproteasi sono specializzate nell'idrolisi dei legami interni delle catene peptidiche, scomponendo le grosse molecole in catene più brevi. Le esoproteasi agiscono invece esclusivamente sui legami peptidici terminali, producendo la liberazione dei singoli amminoacidi. L'azione delle endoproteasi, producendo numerosi peptidi di dimensioni ridotte, fornisce un maggior numero di siti di attacco per le esoprotoeasi, favorendone il lavoro.
Nei mammiferi la digestione delle proteine inizia nello stomaco, grazie ad un enzima detto Pepsina, in grado di lavorare in maniera ottimale in condizioni di pH acido, e pertanto favorito dall'acidificazione prodotta dall' HCl presente nello stomaco.
Le grosse molecole peptidiche, scomposte in molecole più piccole dalla pepsina, vengono poi lavorate nell'intestino da enzimi di origine pancreatica che riducono ulteriormente la dimensione delle catene, per poi essere definitivamente scomposte in amminoacidi da enzimi associati strettamente alla membrana delle cellule dell'epitelio intestinale.
Carboidrasi
La digestione dei carboidrati è affidata a enzimi che attaccano i legami glicosidici scomponendo i polisaccaridi in catene più brevi e poi riducendo queste ultime alle singole unità monosaccaridiche di cui essi sono composti.
Alla classe delle carboidrasi appartengono due categorie di enzimi: le polisaccaridasi, che attaccano le lunghe catene come il glicogeno, l'amido e la cellulosa scomponendole in disaccaridi come il fruttosio, il lattosio, il maltosio o il saccarosio. Questi ultimi vengono ulteriormente scomposti nei rispettivi monosaccaridi grazie all'idrolisi dei legami glicosidici ad opera degli enzimi appartenenti all'altra categoria di carboidrasi, detti glicosidasi.
La principale polisaccaridasi nella maggior parte dei viventi è l'amilasi, in grado di scomporre l'amido, il polisaccaride di riserva più diffuso. Nei vertebrati le amilasi sono prodotte dalle ghiandole salivari, pancreatiche e gastriche. Negli invertebrati invece queste molecole sono in genere prodotte a livello intestinale oltre che salivare.
Un altro enzima di grande importanza per tutta la catena trofica è costituito dalla cellulasi. Questo enzima è in grado di scomporre la cellulosa, un polisaccaride strutturale presente nella parete cellulare di quasi tutti i vegetali e che rappresenta una fonte molto importante di energia che senza questo tipo di enzimi rimarrebbe inutilizzata e non sarebbe in grado di passare da un livello trofico al successivo.
Nonostante la grande importanza rivestita dal punto di vista ecologico da questo enzima, gli organismi pluricellulari che sono in grado di sintetizzarlo sono molto pochi: un mollusco (Teredo navalis), un crostaceo isopode (Limnoria sp.) ed un insetto, comunemente ritrovato nei libri, noto con il nome comune di pesciolino d'argento (Lepisma saccharina).
Nella quasi totalità degli erbivori, tuttavia, la capacità di digerire la cellulosa è garantita dalla simbiosi con batteri che possiedono questi enzimi. Tale processo di simbiosi coinvolge specie molto diverse tra loro e ceppi batterici molto differenti, a riprova di come questo evento, ossia l'acquisizione per simbiosi batterica della capacità di digerire la cellulosa, si sia ripetuta molte volte nella storia della vita sulla terra in maniera del tutto indipendente. Non è, questa, una scoperta sorprendente, considerato l'enorme vantaggio che deriva da questa forma di simbiosi.
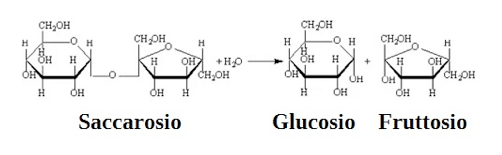
Figura 2: Idrolisi del Saccarosio ad opera della glicosidasi specifica.
Lipasi
Le lipasi sono gli enzimi digestivi coinvolti nella digestione dei lipidi, cioè dei grassi. Poiché i lipidi non sono solubili in acqua, la loro digestione richiede dei passaggi preliminari che creino le condizioni per poter essere scomposti e assimilati. Il passaggio chiave è dato dall'emulsione delle grosse molecole lipidiche, cioè la loro dispersione in acqua sotto forma di piccole goccioline.
Tale fenomeno avviene grazie ad un duplice lavoro: l'azione meccanica operata dai movimenti che avvengono nei distretti digestivi, coadiuvata dall'azione chimica di sali biliari e lecitina. In particolare i sali biliari, che lavorano in ambiente neutro o leggermente basico, svolgono un ruolo fondamentale e la loro presenza è determinante.
I sali biliari sono molecole anfipatiche, possiedono cioè una porzione polare idrofila ed una porzione apolare idrofoba. Le catene lipidiche si legano alle porzioni idrofobe dei sali biliari e si riuniscono insieme formando delle strutture sferiche dette micelle, in cui le porzioni polari dei sali sono rivolte all'esterno e le catene lipidiche legate alle estremità apolari sono rivolte all'interno.
La dimensione dei nuclei lipidici delle micelle è di sei ordini di grandezza inferiore a quella delle semplici goccioline emulsionate senza l'azione dei sali. Ciò garantisce un substrato attaccabile da parte delle lipasi molto più esteso.
Nei vertebrati le lipasi sono secrete dal pancreas, mentre negli invertebrati sono prodotte direttamente dalle cellule dell'intestino.
La presenza dei sali biliari è talmente importante che, in assenza i questi ultimi, i lipidi sono digeriti solo parzialmente e non vengono assorbiti ma prendono la via del colon per essere espulsi attraverso le feci.
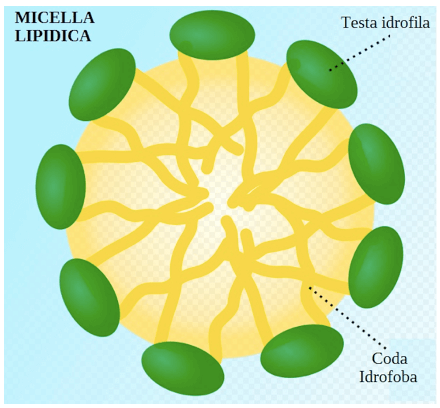
Figura 3: Struttura di una micella lipidica.
Enzimi digestivi secondari
Oltre alle tre classi di enzimi digestivi principali, indispensabili per il assorbimento dei principi nutritivi, esistono altri gruppi di enzimi di minore importanza. Questi sono essenzialmente le esterasi, che idrolizzano il legame estereo e gli enzimi che idrolizzano gli acidi nucleici e i loro derivati, quali le nucleasi, le nucleotidasi e le nucleosidasi.
Questi gruppi di enzimi digestivi non sono indispensabili per la nutrizione e la loro mancanza non ha effetti definitivi sulle capacità nutrizionali dell'organismo. Tuttavia la loro presenza consente una maggiore efficienza del processo metabolico e quindi rappresenta un vantaggio di tipo competitivo.
Link correlati:
Che cosa è un isoenzima?
Che cosa sono gli Eubatteri?
Studia con noi