Dualismo onda particella
Che cosa si intende per dualismo onda particella?
Esperimenti come quello della diffrazione o dell'interferenza provano che la luce si comporta come un'onda elettromagnetica a tutti gli effetti.
Possiamo dunque affermare con certezza che la luce è certamente un'onda.
Tuttavia ci sono casi in cui la luce si comporta come se fosse costituita da particelle; esperimenti come quelli che riguardano l'effetto fotoelettrico o l'effetto Compton non possono essere spiegati se non considerando la luce composta da particelle che prendono il nome di fotoni e sono caratterizzati da una ben precisa energia che dipende dalla frequenza dell'onda come stabilito dalla relazione di Planck:
E = h∙ f
in cui h è la costante di Planck che vale 6,626∙10-34 J∙s ed f è la frequenza dell'onda elettromagnetica.
In analogia a questa duplice natura della luce nel 1924 De Broglie ipotizzò lo stesso tipo di comportamento anche per la materia e per le particelle cariche come per esempio gli elettroni.
Anche per l'elettrone si può considerare che esista un comportamento ondulatorio necessario a spiegare esperimenti come quello della doppia fenditura dove gli elettroni si comportano proprio come se fossero onde producendo figure di interferenza tipiche proprio delle onde.
La caratteristica dell'onda associata alla particella è di avere una frequenza che è data dall'energia della particella diviso la costante di Planck:
f = E / h
mentre la lunghezza d'onda λ, detta lunghezza d'onda di De Broglie, risulta pari alla costante di Planck diviso la quantità di moto della particella:
λ = h / p
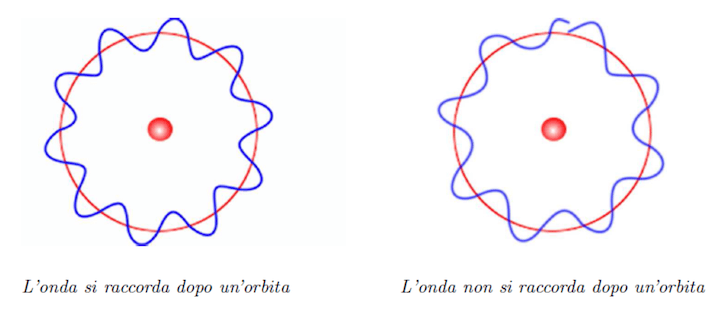
In particolare, nel caso di un elettrone che si muove in un atomo, le traiettorie permesse per la particella sono discrete in quanto essendo l'elettrone un'onda deve valere il principio che l'onda deve raccordarsi nell'orbita.
Questo può accadere solo se la lunghezza dell'orbita sia pari a un numero intero di lunghezze d'onda associate all'elettrone cioè se:
2 · π · r = n · λ
in cui r è il raggio dell'orbita, n è un numero naturale e λ la lunghezza d'onda.
Pertanto i raggi delle orbite nelle quali si trovano gli elettroni risultano discrete ovvero quantizzate e ad ogni raggio permesso corrisponde un livello discreto di energia.
Queste sono configurazioni corrispondenti ad onde stazionarie per cui alla particella elettrone sarà associata un'onda che è un'onda stazionaria per il sistema.
Un'onda stazionaria è un'onda che non si propaga nello spazio ma soggetta soltanto a una modifica dell'ampiezza nel tempo.
La conferma sperimentale dell'ipotesi di De Broglie avvenne nel 1927 durante un esperimento svolto da Davisson e Germer in cui per caso fu osservata la diffrazione di elettroni da una lamina di metallo. La diffrazione è un fenomeno tipico delle onde.
Il comportamento ondulatorio delle particelle diventa significativo quando tra la particella ed il bersaglio sono presenti degli ostacoli come delle fenditure o delle aperture che sono dello stesso ordine di grandezza o più piccoli della lunghezza d'onda della radiazione associata alla particella che si sta studiando.
La lunghezza d'onda tipicamente associata agli elettroni è dell'ordine di grandezza di 0,1 nm (tale valore varierà a seconda dell'energia cinetica degli elettroni) e dunque quando l'elettrone incontrerà nella sua traiettoria ostacoli che hanno questo ordine di grandezza allora diventeranno evidenti le proprietà ondulatorie dell'onda associata alla particella.
Molti materiali presentano un reticolo cristallino nella loro struttura atomica ovvero mostrano una disposizione di atomi organizzati nello spazio in un modo ordinato e la distanza tra gli atomi è sempre dell'ordine di 0,1 nm quindi possiamo avere degli effetti di diffrazione osservabile nel caso in cui elettroni incidano sulla superficie di tali materiali.
Effetti di diffrazione sono dovuti anche a particelle più grandi degli elettroni come per esempio i neutroni o i nuclei.
In realtà a tutta la materia è possibile associare un'onda e pertanto ad ogni particella, indipendentemente dalla sua massa, può essere associata un'onda.
Tuttavia la lunghezza d'onda di quest'onda associata alla particella dipende dalla quantità di moto della particella stessa e quindi dalla sua massa (ricordiamo che la quantità di moto è in modulo pari al prodotto della massa della particella per il modulo della sua velocità).
Se tale lunghezza d'onda risulta molto piccola non sarà possibile però trovare degli ostacoli in natura con i quali si manifesti la natura ondulatoria della particella.
Consideriamo ad esempio una particella con una massa da 1µg (10-6 g): se calcoliamo la sua lunghezza d'onda di De Broglie otteniamo un valore dell'ordine di 10-19 m.
Una dimensione del genere risulta molto più piccola addirittura della dimensione di un nucleo di un atomo che è dell'ordine di 10-15 m e quindi non sarà possibile per una particella di questo tipo osservare fenomeni di diffrazione o interferenza.
In conclusione secondo l'ipotesi di De Broglie la natura presenta una simmetria ben precisa: così come la luce può essere un'onda oppure si può comportare come un insieme di particelle dette fotoni così anche le particelle cariche come gli elettroni o in generale la materia si può comportare come un'onda.
Link correlati:
Che cos'è la massa relativistica?
Spiegazione dell'esperimento di Franck-Hertz
Cosa rappresenta l'equazione E = m ∙ c2?
Che cosa sono i bosoni?
Studia con noi