Semiconduttori
Generalità e proprietà dei semiconduttori
I semiconduttori sono sostanze solide la cui conducibilità elettrica è intermedia fra quella di un metallo e quella di un isolante. Pertanto un semiconduttore è un materiale che non conduce l'elettricità bene come un conduttore (che dispone di molti elettroni di conduzione) liberi di muoversi al loro interno, però lo fa meglio di un isolante.
Sono semiconduttori il silicio e il germanio, che a temperatura molto bassa si comportano come isolanti, mentre a temperatura ambiente alcuni elettroni acquistano abbastanza energia da consentire il passaggio di una debole corrente elettrica.
Semiconduttori di tipo n e di tipo p
Il numero di questi elettroni, i portatori di carica, può essere ulteriormente aumentato se si inseriscono nel semiconduttore un certo numero di atomi di tipo diverso, cioè il materiale viene "drogato" con impurità.
La struttura del silicio o del germanio è regolare; ogni atomo è legato ad altri 4 vicini. Se si sostituiscono alcuni atomi di silicio con atomi di arsenico, per esempio, il numero di elettroni di conduzione aumenta; l'arsenico è, infatti, un donatore di elettroni, perché possiede 5 elettroni nel guscio più esterno, 4 dei quali si legano agli atomi della struttura del silicio, mentre uno resta libero e si aggiunge ai portatori di carica. Poiché gli elettroni hanno carica negativa, un semiconduttore così drogato si dice di tipo n.
Se, invece, si aggiungono al silicio degli atomi di boro, si verifica un fenomeno più strano. Il boro ha solo 3 elettroni esterni, e quindi si lega a 3 atomi di silicio; il quarto legame è "vuoto", e costituisce una lacuna nel materiale. Un elettrone di un altro atomo può occupare questo spazio libero, ma nel farlo crea un altro spazio nel punto da cui si è mosso: è come se la lacuna si fosse spostata in direzione opposta a quella del moto dell'elettrone.
Ma un moto di cariche negative in un verso equivale a un moto di cariche positive in verso opposto, e quindi è come se le lacune fossero cariche positivamente. I materiali come il boro si dicono accettori, e il semiconduttore drogato in questo modo si dice di tipo p.
Unendo un semiconduttore di tipo n e uno di tipo p si ottiene una giunzione p-n, su cui si basano i diodi e i transistor a semiconduttore, elementi che sono i costituenti essenziali dei circuiti integrati, contenuti in tutte le apparecchiature elettroniche moderne.
In sintesi: i circuiti integrati, componenti di base di apparecchi elettronici e computer, sono formati da un gran numero di diodi e transistor a semiconduttore, a loro volta ottenuti da giunzioni p-n, realizzate avvicinando molto intimamente un semiconduttore di tipo p e uno di tipo n.
Conduzione nei semiconduttori
La corrente elettrica è di solito dovuta al solo moto degli elettroni; la conduzione nei metalli e quella nei semiconduttori si distinguono essenzialmente per le bande di energia occupate dagli elettroni di conduzione. In un cristallo metallico gli elettroni di valenza degli atomi che lo costituiscono sono distribuiti su orbitali estesi a tutto il cristallo, su ciascuno dei quali possono esistere (per il principio di Pauli) soltanto 2 elettroni.
Questi orbitali costituiscono i livelli energetici su cui si trovano gli elettroni che danno luogo al legame metallico.
Il numero degli orbitali metallici è straordinariamente grande (ed è pari al numero di atomi che costituiscono il cristallo) e la differenza di energia fra due orbitali successivi è straordinariamente piccola.
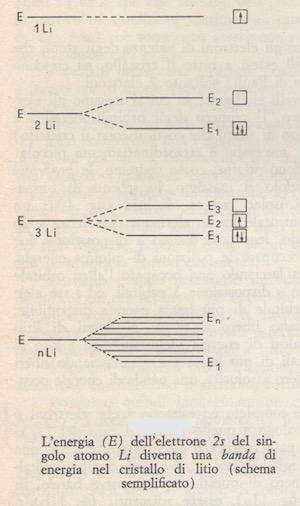
Consideriamo ora, semplificandolo al massimo, lo schema di formazione di un cristallo metallico da atomi isolati, ad esempio di litio.
Un atomo isolato di litio nel suo stato fondamentale ha un elettrone di valenza sullo strato 2s, di energia E (si veda figura seguente).
Due atomi di litio, legandosi, hanno a disposizione due orbitali, e poiché gli elettroni vanno ad occupare le posizioni di minima energia, essi occupano l'orbitale di minima energia lasciando non occupato l'altro orbitale possibile.
Tre atomi di litio legandosi hanno a disposizione 3 orbitali, ed i tre elettroni di valenza occupano totalmente l'orbitale di più bassa energia disponibile, parzialmente l'orbitale successivo e lasciano libero il terzo.
N atomi di litio avranno a disposizione N orbitali, con valori di energia vicinissimi, ed i loro N elettroni di valenza occuperanno gli orbitali di più bassa energia, lasciando liberi gli altri.
Si ha così nel caso del litio (allo zero assoluto), una banda di energie occupata per metà, detta banda di valenza.
Se in una specie atomica lo stato s è completo ed esistono anche elettroni p (ad esempio Al: 3s2 3p), con ragionamento analogo a quello fatto nel caso del Li, si ha una banda di energia totalmente occupata costituita dagli elettroni s ed una banda successiva costituita dall'insieme degli elettroni p, che sarà occupata totalmente o parzialmente a seconda del numero di questi.
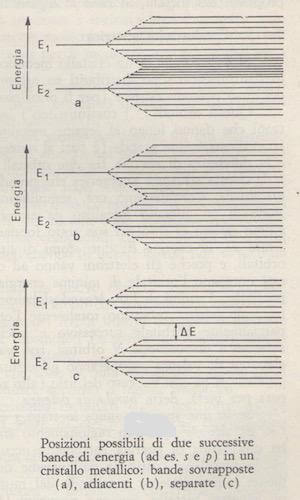
Le successive bande, in un generico metallo, possono sovrapporsi, essere adiacenti o essere separate da una differenza di energia AE. Inoltre, gli elettroni di valenza degli atomi che costituiscono il cristallo possono occupare totalmente o parzialmente i livelli a disposizione, e ciò è determinante agli effetti della conduttività elettrica.
Se mediante una pila elettrica si stabilisce una differenza di potenziale fra due punti di un metallo, cioè si crea fra essi un campo elettrico, gli elettroni subiscono una istantanea accelerazione (cui corrisponde un aumento del loro contenuto di energia) e iniziano a muoversi nella direzione del campo (passaggio di corrente ).
È chiaro che ciò può avvenire soltanto se gli elettroni sono in grado di poter assorbire detti aumenti di energia, cioè se esistono livelli energetici vuoti (banda di conducibilità) corrispondenti ai loro nuovi, maggiori contenuti di energia.
Ciò si verifica se gli elettroni occupano solo parzialmente la banda di valenza (caso del Li, in cui gli elettroni occupano N/2 orbitali degli N disponibili).
Se la banda di valenza è totalmente occupata, si possono invece avere 3 casi: il cristallo può essere conduttore, non conduttore (isolante), semiconduttore.
- Se la banda totalmente occupata è sovrapposta o è adiacente con la successiva banda vuota, gli elettroni possono passare da un livello all'altro con piccolissima spesa di energia, ed il cristallo è conduttore.
- Se la banda totalmente occupata è separata dalla banda successiva vuota da una zona proibita corrispondente ad un salto di energia AIE possono aversi due casi:
a) se il valore di ΔE è elevato (alcuni eV) il cristallo è non conduttore (isolante), e non è quindi un metallo (ad esempio il diamante: 7 eV);
b) se il valore di ΔE non supera 1,5 eV, allora è possibile, con una ragionevole spesa di energia, far passare elettroni dalla banda piena alla banda vuota, ed il cristallo è un semiconduttore (ad esempio germanio 0,72 eV, silicio 1,1 eV).
Quanto ora detto spiega perché nei semiconduttori ad un aumento di temperatura, cioè dell'energia media degli elettroni, corrisponde un aumento di conduttività elettrica, e perché per essi non sia valida la legge di Ohm.
Semiconduttori impuri o estrinseci
Il meccanismo di semiconduzione ora descritto si riferisce a semiconduttori puri (o intrinseci).
Aggiungendo ad un semiconduttore puro piccole quantità di atomi diversi da quelli che lo costituiscono, e che possiedano particolari caratteristiche elettroniche (rendendo così difettivo il reticolo cristallino), si hanno semiconduttori impuri o estrinseci, con proprietà particolari dovute ai nuovo livelli energetici introdotti dagli atomi aggiunti.
Studia con noi