Stato Fondamentale
Significato di stato fondamentale
Lo stato fondamentale di un atomo o di una molecola è lo stato a minor energia.
Da un punto di vista elettronico esso corrisponde alla configurazione elettronica che è possibile scrivere seguendo l'ordine di riempimento degli orbitali dettato dalla regola della diagonale:
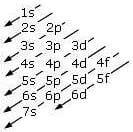
Regola della diagonale: indica l'ordine di riempimento dei sottolivelli.
Si comincia dal sottolivello 1s e poi si seguono le frecce, verso il basso.
Secondo il modello atomico di Bohr, quando, nel caso dell'atomo di idrogeno, l'elettrone ruota sulla prima orbita non assorbe e non emette energia e si trova nel suo stato fondamentale.
Solo assorbendo energia l'elettrone può saltare su orbite di energia superiore. L'atomo passa dallo stato fondamentale allo stato eccitato.
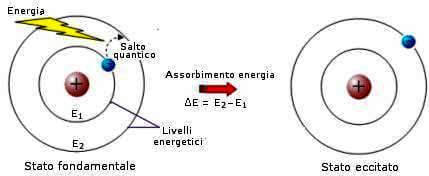
Assorbimento di energia da parte dell'atomo con formazione di uno stato eccitato
La configurazione elettronica più stabile per l'atomo di idrogeno è la seguente:
1s1
che corrisponde anche alla configurazione elettronica del suo stato fondamentale.
Nel caso in cui l'elettrone più esterno si trovi su un orbitale di energia superiore, ad esempio:
2s1
l'atomo si trova in uno stato eccitato.
Nel caso dell'atomo di sodio, la configurazione elettronica più stabile è la seguente:
1s2 2s2 2p6 3s1
che corrisponde anche alla configurazione elettronica del suo stato fondamentale.
Nel caso in cui l'elettrone più esterno si trovi su un orbitale di energia superiore, ad esempio:
1s2 2s2 2p6 4s1
l'atomo si trova in uno stato eccitato.
Link correlati:
Che cosa si intende per emissione stimolata?
Qual è la differenza tra uno spettro continuo e uno spettro a righe?
Studia con noi