Calore latente acqua
Calore latente di ebollizione e di fusione dell'acqua
Vuoi sapere cosa rappresenta il calore latente dell'acqua?
Vuoi sapere quanto vale il calore latente dell'acqua?
Se si continua con la lettura dell'articolo.
La legge fondamentale della termologia afferma che fornendo (o sottraendo) calore a una certa quantità di acqua, si ottiene un riscaldamento (o un raffreddamento) dell'acqua stessa.
L'esperienza però ci insegna che non è sempre così. Per esempio, inserendo un termometro all'interno di una massa d'acqua che sta bollendo, pur continuando a fornire calore, la massa d'acqua - durante l'ebollizione - rimane sempre alla temperatura di 100°C (alla pressione di 1 atmosfera).

Durante l'ebollizione dell'acqua la temperatura rimane fissa a 100°C (alla pressione di 1 atm).
Stessa cosa succede durante la fusione di un cubetto di ghiaccio: pur sottraendo calore dall'ambiente circostante, durante la fusione, la temperatura del cubetto di ghiaccio rimane costante a 0°C (alla pressione di 1 atmosfera).
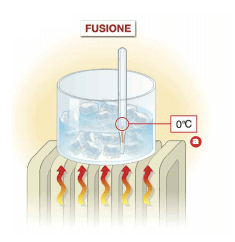
Durante la fusione del ghiaccio la temperatura rimane fissa a 0°C (alla pressione di 1 atm).
Pertanto, durante la fusione o l'ebollizione dell'acqua la temperatura rimane costante rispettivamente a 0°C o a 100°C (alla pressione di 1 atm).
Il calore fornito in questi passaggi di stato è definito latente ovvero "nascosto" (dal latino latere, restare nascosto) perché, come detto in precedenza, l'assorbimento di calore non si manifesta con un aumento della temperatura.
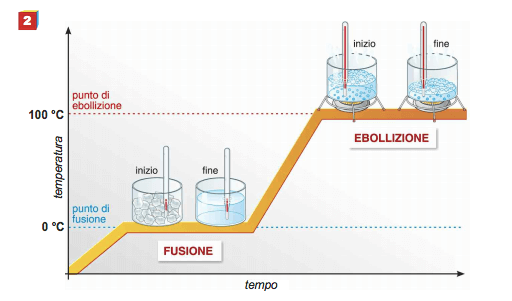
Curva di riscaldamento dell'acqua distillata: si nota che durante la fusione (tratto B-C) e durante l'ebollizione (tratto D-E) la temperatura rimane costante. Il calore fornito in questi passaggi di stato è definito latente.
Definizione di calore latente di fusione del ghiaccio
Il calore latente di fusione del ghiaccio (λf) è la quantità di energia necessaria per fondere completamente 1 g di ghiaccio alla temperatura di fusione che, come è noto, è di 0°C.
Il calore assorbito nella fusione viene utilizzato per vincere le forze di coesione che mantengono le molecole fisse, vicine le une alle altre.
Definizione di calore latente di ebollizione del ghiaccio
Come la fusione, anche l'ebollizione è un processo che richiede energia. Il calore latente di ebollizione (λe) è la quantità di energia necessaria per far evaporare completamente 1 grammo di sostanza alla temperatura di ebollizione (100°C alla pressione di 1 atmosfera).
Il calore latente di ebollizione viene impiegato per indebolire le forze di coesione tra le particelle del liquido, permettendo loro di allontanarsi fino a passare allo stato di vapore.
Quanto valgono il calore latente di fusione dell'acqua e il calore latente di ebollizione dell'acqua?
Il calore latente di fusione dell'acqua misurato in joule su grammo di acqua (J/g) è il seguente:
calore latente di fusione dell'acqua = 333,5 J/g
Nel Sistema Internazionale il calore latente viene invece misurato in J/kg; in tal caso il calore latente di fusione dell'acqua corrisponde a 3,335 · 105 J/kg.
Il calore latente di ebollizione dell'acqua misurato in joule su grammo di acqua (J/g) è il seguente:
calore latente di ebollizione dell'acqua = 2272 J/g
Espresso in J/kg il calore latente di ebollizione dell'acqua corrisponde a 2,272 · 106 J/kg
Gli elevati valori del calore latente dell'acqua dipendono direttamente dal legame a idrogeno che mantiene assieme le molecole di acqua e tende ad ostacolare il loro movimento, ossia a contenere la loro energia cinetica direttamente legata alla temperatura del liquido.
Calori latenti e passaggi di stato dell'acqua
Ad ogni passaggio di stato dell'acqua corrisponde un proprio calore latente.
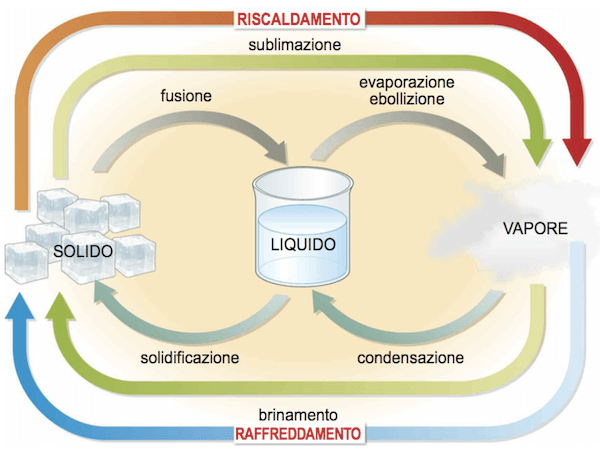
Passaggi di stato.
Abbiamo già visto in precedenza i calori latenti di fusione e di ebollizione dell'acqua.
Per la condensazione si ha il calore latente di condensazione dell'acqua; esso è numericamente uguale ma di segno opposto al calore latente di ebollizione dell'acqua.
Per la solidificazione si ha il calore latente di solidificazione dell'acqua ; esso è numericamente uguale ma di segno opposto al calore latente di fusione dell'acqua.
Calore latente molare di fusione dell'acqua e calore latente molare di ebollizione dell'acqua
Nel caso in cui il calore latente dell'acqua venga espresso per mole di sostanza e non per grammo, si parla di calore latente molare di fusione dell'acqua e di calore latente molare di ebollizione dell'acqua. Nel Sistema Internazionale il calore latente molare si esprime pertanto in J/mol.
Si ha che:
calore latente molare di fusione dell'acqua = 6.008,1 J/mol
e
calore latente molare di ebollizione dell'acqua = 40.930,7 J/mol
Esercizio
Si calcoli il calore necessario per fondere completamente un cubetto di ghiaccio di massa 10 grammi che si trova alla temperatura di 0°C e alla pressione di 1 atmosfera. Si sappia che il calore latente di fusione del ghiaccio è pari a 333,5 J/g.
Svolgimento
Il calore latente di fusione del ghiaccio indica la quantità di calore necessaria per fondere un grammo di ghiaccio che si trova alla temperatura di 0°C.
Per calcolare il calore necessario per fondere una quantità di ghiaccio di massa m, è sufficiente moltiplicare il calore latente di fusione del ghiaccio per il valore della massa m in grammi, ovvero:
Q = m ·λf
in cui:
m = massa del ghiaccio (g)
λf = calore latente di fusione del ghiaccio (J/g)
Q = quantità di calore fornita la ghiaccio (J)
Nel nostro caso:
m = 10 g
λf = 333,5 J/g
Q = ?
Sostituendo in modo opportuno i dati a nostra disposizione, si ha che:
Q = m · λf = 10 · 333,5 = 3.335 J
Pertanto sono necessari 3.335 J per fondere completamente 10 g di ghiaccio.
Link correlati:
Quanto vale a capacità termica dell'acqua?
Quanto vale il calore specifico del vapore acqueo?
Che cos'è e come è fatta la curva di raffreddamento di una sostanza pura?
Studia con noi