Da solido a vapore
Passaggio di stato da solido a vapore
La materia può esistere in tre diversi stati di aggregazione che sono: solido (come il ghiaccio), liquido (come l'acqua) e aeriforme (come l'aria).
Mediante variazioni di pressione e/o di temperatura la materia può inoltre modificare il proprio stato di aggregazione: le trasformazioni conseguenti, che sono trasformazioni fisiche e quindi trasformazioni reversibili della materia, sono dette passaggi di stato.
In questa lezione, dopo avere brevemente introdotto sia lo stato solido che lo stato vapore, vedremo come si chiama il passaggio dallo stato solido a quello aeriforme e come si può ottenere tale trasformazione.
Stato solido e stato aeriforme
Come detto in precedenza lo stato solido è uno dei tre stati di aggregazione della materia: una sostanza allo stato solido è caratterizzata da volume proprio e forma propria.
Le particelle di una sostanza allo stato solido sono tenute insieme da forze attrattive tali da bloccarle in posizione fisse.
Il vapore è invece un particolare stato aeriforme della materia; si differenzia da un gas in quanto si trova al di sotto della sua temperatura critica (per ulteriori info: differenza tra vapore e gas).
Volume e forma di una sostanza che si trova allo stato di vapore dipendono dal recipiente che la contiene. Le particelle di una sostanza allo stato di vapore sono inoltre animate da moto caotico.
Ma come si chiama il passaggio di stato da solido a vapore?
Il passaggio di stato da solido a vapore è detto sublimazione: tale trasformazione avviene direttamente tra i due stati fisici della materia senza quindi passare attraverso lo stato liquido.
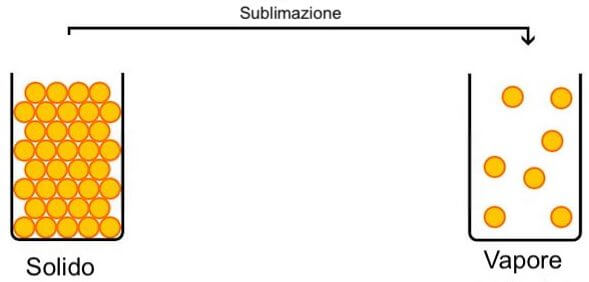
La sublimazione è il passaggio dallo stato solido a quello vapore. Tale trasformazione avviene con acquisto di calore ed è quindi un processo endotermico.
Sono poche le sostanze che in natura possono sublimare: tra esse ricordiamo lo iodio, la naftalina, la canfora e il ghiaccio secco (anidride carbonica solida).
La sublimazione è una trasformazione reversibile della materia: ciò significa che raffreddando il vapore ottenuto durante il processo di sublimazione si può riottenere il solido di partenza: tale passaggio di stato, opposto alla sublimazione, è noto come brinamento.
Come detto in precedenza, per poter sublimare una sostanza è necessario fornire calore: poiché il calore ceduto alla sostanza non provoca innalzamento della temperatura del solido ad esso è attribuito l'aggettivo latente (= che non si manifesta con alcun segno o sintomo esterno): si parla così di calore latente di sublimazione (λsub) la cui unità di misura, nel Sistema Internazionale, è J·g-1.
Il calore latente di sublimazione corrisponde alla quantità di calore necessaria per sublimare 1 grammo di sostanza alla temperatura di sublimazione.
Riassumendo
1) Il passaggio dallo stato solido a quello liquido è detto sublimazione
2) La sublimazione è un processo endotermico che avviene quindi con acquisto di calore
3) La sublimazione è una trasformazione reversibile della materia
4) Sono poche le sostanze che possono sublimare; tra essere ricordiamo lo iodio
5) Il passaggio opposto alla sublimazione è il brinamento
6) Il calore latente di sublimazione è la quantità di energia necessaria per sublimare 1 g di sostanza alla temperatura di sublimazione
Link correlati:
Quiz online sulla materia
Passaggio di stato da liquido a solido
Passaggio di stato da solido a liquido
Passaggio di stato da gas a solido
Studia con noi