Configurazione elettronica del carbonio
Come scrivere la configurazione elettronica del carbonio
La configurazione elettronica del carbonio indica la disposizione degli elettroni negli orbitali di questo elemento chimico.
Per scrivere la configurazione elettronica del carbonio (così come di qualsiasi altro elemento) bisogna seguire la regola della diagonale, che indica la sequenza di riempimento degli orbitali.
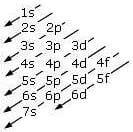
Inoltre bisogna ricordare che nell'orbitale s possono essere collocati al massimo 2 elettroni, nell'orbitale p possono essere collocati al massimo 6 elettroni, nell'orbitale d possono essere collocati al massimo 10 elettroni, ecc.
Infine bisogna sottolineare il fatto che vi sono diversi modo per scrivere la configurazione elettronica del carbonio.
Il metodo che useremo in questa sede permette di rappresentarla in modo sintetico, scrivendo gli elettroni ad esponente della sigla che identifica l'orbitale.
In base a queste considerazioni, la configurazione elettronica del carbonio è:
1s2 2s2 2p2
Infatti il numero atomico del carbonio è Z = 6, quindi l'atomo di carbonio ha 6 protoni e 6 elettroni.
Seguendo la regola della diagonale, si capisce che i primi due elettroni si posizionano sull'orbitale 1s, altri due elettroni si posizionano nell'orbitale 2s e i restanti due nell'orbitale 2p.
La configurazione elettronica esterna del carbonio, quella relativa agli elettroni di valenza è invece la seguente: 2s2 2p2.
Come si può notare, il carbonio ha solo due orbitali 2p semipieni (si ricordi che gli orbitali p sono in totale 3 ciascuno dei quali contiene al massimo due elettroni) e, pertanto, dovrebbe dare origine solamente a due legami covalenti.
In realtà il carbonio è prevalentemente tetravalente, cioè in grado di formare 4 legami con altri atomi.
Si suppone pertanto la promozione di un elettrone dall'orbitale 2s all'orbitale 2p vuoto e la successiva ibridazione orbitalica.
La configurazione elettronica del azoto (Z = 7) è simile a quella del carbonio (Z = 6); in più c'è solo un elettrone collocato nell'orbitale 2p.
Altri esercizi simili:
Qual è configurazione elettronica del potassio?
Qual è configurazione elettronica del calcio?
Che cos'è l'ibridazione sp3 del carbonio?
Studia con noi