Regola della diagonale
Spiegazione della regola della diagonale
La determinazione della configurazione elettronica di ciascuna specie atomica nel suo stato fondamentale è di straordinaria importanza in chimica perché; tali configurazioni condizionano la formazione dei legami chimici fra gli atomi per formare le molecole.
A tale scopo è importante conoscere la sequenza esatta con la quale vengono riempiti i sottolivelli di energia, ovvero la sequenza con cui gli elettroni vanno ad occupare i sottolivelli energetici.
Rappresentazione della regola della diagonale
L'ordine di riempimento dei sottolivelli di energia può essere ricordato seguendo la regola della diagonale che è rappresentata qui di seguito:
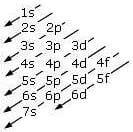
È sufficiente seguire le linee oblique dall'alto verso il basso per ricordare la sequenza con cui vengono riempiti i sottolivelli di energia.
La sequenza dettata dalla regola della diagonale è la seguente:
1s → 2s → 2p → 3s → 3p → 4s → 3d → 4p → 5s → 4d → ecc.
Nello scrivere la configurazione elettronica di un elemento chimico bisogna inoltre ricordare che:
- il sottolivello s (1s, 2s, 3s, ecc.) può contenere al massimo 2 eletttroni;
- il sottolivello p (2p, 3p, 4p, ecc.) può contenere al massimo 6 elettroni;
- il sottolivello d (3d, 4d, 5d, ecc.) può contenere al massimo 10 elettroni.
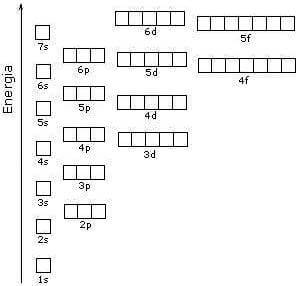
Utilizzando i quadratini per rappresentare i vari orbitali energetici, la sequenza di riempimento può essere rappresentata anche nel seguente modo:
Studia con noi