Combustione
Reazione chimica di combustione
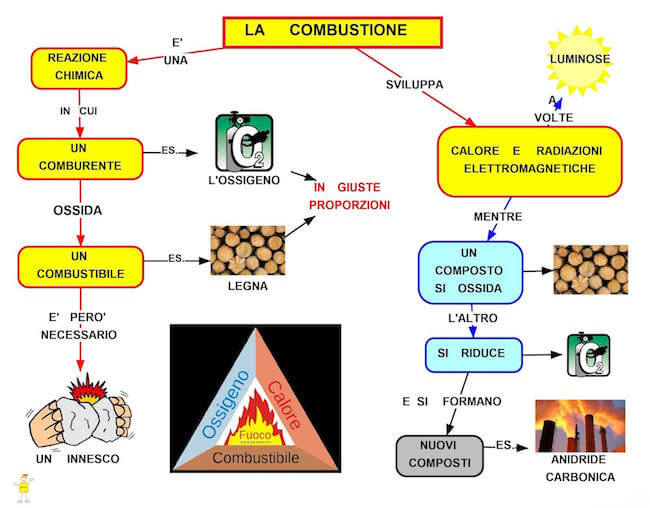
Con il termine combustione si indica un processo di ossidazione rapido, che avviene con emissione di luce e di calore (fiamma), durante il quale l'energia chimica si degrada in energia termica.
Generalmente quando si parla di combustioni ci si riferisce a reazioni di ossidazione rapida mediante ossigeno (ad esempio la combustione del metano), ma sono combustioni anche ossidazioni rapide che hanno luogo in assenza di questo gas (ad esempio l'idrogeno brucia con fiamma in ambiente di cloro, formando HCl).
Le reazioni di combustione sono reazioni chimiche per lo più assai complesse, specialmente nel caso di combustibili gassosi, perché generalmente costituite da catene di reazioni, di norma ramificate.
Così la combustione dell'idrogeno in presenza di ossigeno per formare acqua, apparentemente semplicissima (2H2 + O2 → 2H2O), comporta in realtà numerose reazioni intermedie e collaterali, con formazione di atomi e di radicali.
Il calore prodotto in una reazione di combustione è detto calore di combustione.
Influenza della temperatura sulla velocità di reazione
Una reazione di combustione, come avviene per la gran parte dei casi, aumenta la propria velocità con l'aumentare della temperatura: per bassi valori di temperatura le combustioni avvengono lentamente e quindi senza rapido sviluppo di calore, che viene dissipato man mano che si produce (combustioni lente: ad esempio combustioni biologiche).
Esiste una soglia di temperatura (temperatura di ignizione) oltre la quale inizia la combustione vera e propria con emissione di luce e di calore.
Le combustioni lente possono quindi trasformarsi spontaneamente in combustioni rapide (processo di autocombustione) se la quantità di calore da esse sviluppato non viene sufficientemente dissipata man mano che si produce.
Si genera in tal caso un meccanismo a catena: la temperatura aumenta, e ciò fa aumentare la velocità di reazione e quindi la quantità di calore sviluppato nell'unità di tempo; di conseguenza aumenta ancora la temperatura, e quindi la velocità di reazione; e così via.
Con questo meccanismo può raggiungersi la temperatura di ignizione, alla quale la massa inizia a bruciare (autocombustione di pagliai, legnaie, depositi di cascami tessili ecc.).
Il processo di autocombustione non è frequente, e molte autocombustioni sono in realtà incendi colposi o dolosi.
Tipologie di combustibili utilizzati nelle reazioni di combustione
Il processo di combustione può aver luogo con combustibili solidi, combustibili liquidi e combustibili gassosi; dal punto di vista pratico le combustioni più importanti, e quindi più studiate, sono quelle che avvengono in fase eterogenea solido/gas (ad esempio combustione del carbone all'aria) e in fase omogenea gassosa (ad esempio combustione del metano in aria).
Le combustioni di combustibili liquidi impiegati allo stato di vapore (ad esempio benzina nei motori a scoppio) rientrano nelle combustioni in fase gassosa.
Triangolo del fuoco
Il triangolo del fuoco è un triangolo nel quale vengono rappresentati i tre elementi necessari alla combustione: combustibile, comburente e fonte di innesto (calore).
Detonazione
Indeterminate condizioni può succedere che una miscela gassosa brucia istantaneamente. Si ha in questi casi il fenomeno noto con il nome di "detonazione".
I problemi riguardanti la detonazione di miscele gassose sono di grande importanza per i loro stretti rapporti con il corretto funzionamento dei motori a combustione interna.
Pile a combustione
Le pile a combustione sono particolari pile che sfruttano, per il loro funzionamento, una reazione di combustione.
Link correlati:
Quando una combustione si dice spontanea?
Vuoi sapere perché avvenga la combustione cosa sono necessari?
Che cosa significa il termine combustione?
Come avviene la combustione dell'alluminio?
Studia con noi