Differenza tra legame covalente e ionico
Qual è la differenza tra legame covalente e ionico?
Legame covalente e legame ionico sono entrambi legami chimici; tra i due legami ci sono però sostanziali e importanti differenze, vediamo quali!
Il legame covalente si forma tra atomi che hanno una differenza di elettronegatività inferiore a 1,9, mentre il legame ionico si realizza quando la differenza di elettronegatività tra i due atomi è superiore a 1,9.
Questa è la prima e più importante differenza tra legame covalente e legame ionico; questa differenza ne determina conseguentemente anche altre.
Essendo la differenza di elettronegatività non particolarmente elevata, nel legame covalente si ha - tra i due atomi - una condivisione di elettroni. Il numero di elettroni messi in comune da un atomo è tale da permettergli di raggiungere l'ottetto e quindi la stabilità.
Gli elettroni messi in comune non appartengono più all'uno o all'altro atomo, ma appartengono ad entrambi: si dice che i due elettroni sono stati messi in compartecipazione.
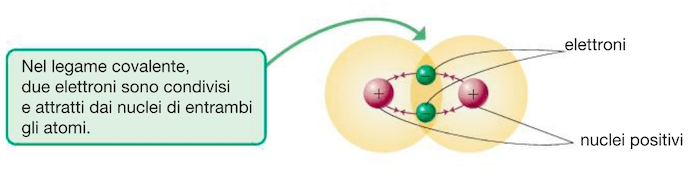
Formazione del legame covalente tra due atomi di idrogeno con conseguente condivisione di due elettroni.
Il legame ionico si realizza quando la differenza di elettronegatività fra i due atomi che intendono legarsi è superiore a 1,9; si verifica il trasferimento di uno o più elettroni dall'atomo meno elettronegativo - che perdendo elettroni diventa uno ione positivo = catione - all'atomo più elettronegativo - che acquistando elettroni diventa uno ione negativo = anione.
Il legame ionico è la conseguenza dell'attrazione elettrostatica che si manifesta tra i due ioni di carica opposta.
Nel legame ionico non si ha quindi condivisione di elettroni come nel legame covalente ma un trasferimento di uno o più elettroni dall'atomo meno elettronegativo a quello più elettronegativo.
Il numero di elettroni che un atomo perde o acquista è tale da permettergli di raggiungere l'ottetto e quindi la stabilità.
Nel cloruro di sodio, ad esempio, il sodio perdendo un elettrone, assume una carica positiva (Na+) e raggiunge la configurazione elettronica del neon (configurazione ad ottetto completo) mentre il cloro, acquistando un elettrone, assume una carica negativa (Cl−) e raggiunge la configurazione elettronica dell'argon (configurazione ad ottetto completo).
Si forma il cloruro di sodio, un composto ionico in cui gli ioni Na+ e gli ioni Cl− risultano uniti tramite legame ionico.
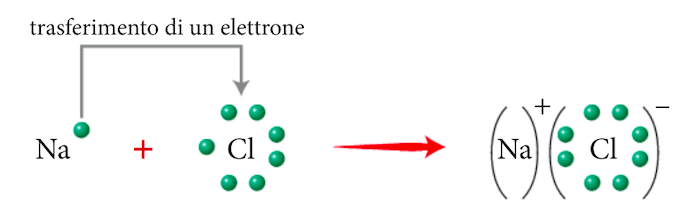
Formazione del legame ionico in NaCl.
Link correlati:
Quiz online sui legami chimici
Che cos'è il legame metallico?
Studia con noi