pH sangue
Regolazione biologica del pH del sangue
I principali costituenti protoplasmici sono proteine estremamente sensibili alle variazioni di acidità del mezzo liquido (sangue, liquido interstiziale dei tessuti) con cui le cellule si trovano a contatto.
Questi liquidi tenderebbero a presentare continue e forti variazioni di acidità dal momento che in essi si versano sostanze derivanti dal metabolismo cellulare aventi carattere spiccatamente acido (ad esempio acido carbonico, acido lattico, ecc.), se non possedessero, il sangue soprattutto, un forte potere tampone.
Qual è il pH del sangue?
La concentrazione degli ioni idrogeno nel sangue è di 4 · IO-8 g/L, che, espressa in termini di pH, corrisponde a un valore uguale a 7,4 (da 7,35 a 7,45, a 37 °C per l'organismo umano): di conseguenza il sangue ha una reazione debolmente alcalina.
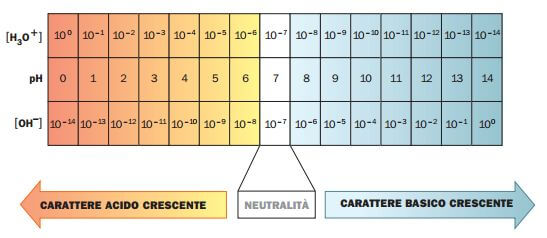
Scala del pH.
Le variazioni del pH del sangue compatibili con la vita sono comprese fra 7,1 e 7,7: queste oscillazioni corrispondono a variazioni del 100% in più o del 50% in meno della concentrazione normale degli ioni idrogeno.
Poiché, invece, le differenze in pH tra sangue arterioso e venoso refluo dai tessuti, nel quale si versano tutti i metaboliti acidi di origine cellulare, non sono mai maggiori di 0,02-0,04 unità pH, e poiché il pH del sangue si mantiene costante anche dopo l'aggiunta sperimentale di forti quantità di acido o di base, se ne deduce che le sostanze tampone in esso presenti sono molto efficaci nell'impedire forti variazioni della reazione del sangue sia in senso acido sia in senso basico.
La regolazione del pH del sangue e in generale dei liquidi organici è affidata non solo all'efficacia dei sistemi tampone presenti, ma anche alla funzione di determinati organi.
L'insufficienza dei meccanismi di regolazione del pH del sangue porta a due gravi conseguenze note con il nome di acidosi (pH < 7,35, si accompagna ad un aumento di acido o a una perdita di basi) e alcalosi (pH > 7,45, si accompagna a un aumento di basi o a una perdita di basi).

pH ottimale del sangue.
Sistemi tampone biologici coinvolti nella regolazione del pH del sangue
I sistemi tampone del sangue sono rappresentati in primo luogo dalle proteine plasmatiche e dalla proteina specifica contenuta nelle emazie, l'emoglobina (Hb).
Queste proteine esplicano un potere tampone perché il loro punto isoelettrico è inferiore al pH del sangue: essendo dissociate prevalentemente come acidi (acidi deboli), i loro ioni hanno carica negativa e possono così costituire un legame salino con gli alcali presenti nel sangue.
Il sistema tampone può essere allora rappresentato dal sistema proteinato sodico - proteina indissociata, ossia da un classico sistema del tipo acido debole-sale dell'acido debole con base forte (H-proteina)-(Na-proteina).
I sistemi tampone del plasma includono anche il sistema bicarbonato - acido carbonico (NaHCO2-H2CO3), il sistema dei fosfati monosodico (NaH2PO4) e bisodico (Na2HPO4) mentre nelle emazie a questi corrispondono i sistemi KHCO3-H2CO3, K2HPO4-KH2PO4: la diversità del catione dipende dalla prevalente concentrazione degli ioni sodio nel plasma e degli ioni potassio all'interno dei globuli rossi.
All'interno di questi corpuscoli, entro i limiti di variazione di pH sopra accennati, il sistema tampone più efficiente è rappresentato dall'emoglobina che vi si trova in alta concentrazione (33%) e ha un punto isoelettrico molto vicino al pH del sangue; passando dallo stato ridotto allo stato ossigenato essa è capace di variare il suo grado di ionizzazione o di dissociazione come acido.
Poiché nel plasma il contenuto in fosfati è molto basso, il sistema NaHCO3-H2CO3 è di gran lunga il più importante.
Apparati connessi al meccanismo di regolazione del pH del sangue
Gli apparati più strettamente connessi al meccanismo di regolazione del pH del sangue sono l'apparato respiratorio con il centro respiratorio e i reni.
L'entrata di H+ nel sangue in determinate condizioni metaboliche (formazione di chetoacidi nel diabete, formazione di acido lattico in forti quantità in un lavoro intenso) si riflette immediatamente in un aumento dell'acido carbonico H2CO3 e conseguentemente dell'anidride carbonica CO2.
Ne deriva, attraverso una stimolazione specifica delle cellule del centro respiratorio bulbare, un aumento della ventilazione polmonare e una più rapida e abbondante eliminazione di CO2.
La CO2 rappresenta perciò la forma volatile ed eliminabile attraverso l'aria espirata dell'H2CO3 formatosi in eccesso.
Importantissima è anche la funzione dei reni nel garantire la costanza del pH del sangue al valore di 7,4. Il filtrato glomerulare è un ultrafiltrato del plasma, di cui ha la medesima composizione, eccetto che per la mancanza delle proteine, la medesima concentrazione di elettroliti e lo stesso pH.
Poiché a pH 7,4 il rapporto NaHCO3/CO2 è circa uguale a 20 e il rapporto Na2HPO4/ NaH2PO4 vale circa 4, l'escrezione di un'urina dello stesso pH del plasma rappresenterebbe una grave perdita di ioni sodio (Na+).
Però, durante il passaggio del filtrato glomerulare lungo i tubuli renali, si produce uno scambio fra gli Na+ presenti nel filtrato glomerulare e gli H+ eliminati dalle cellule dei tubuli e formatisi presumibilmente entro queste dall'idratazione della CO2 ad acido carbonico e dalla sua prima dissociazione che conduce alla formazione appunto di ioni idrogeno e di ioni bicarbonato.
Questo scambio tra Na+ e H+ produrrebbe un'urina estremamente acida se non ci fosse il sistema tampone dei fosfati mono- e bisodici: gli H+ riversatisi nell'urina inducono un aumento dei fosfati monosodici con conseguente acidificazione dell'urina, il cui pH varia normalmente tra 4,8 e 7-7,5.
Tale ampia variazione si deve in massima parte a una variazione del rapporto Na2HPO4/NaH2PO4: nell'urina avente un pH intorno a 5,0-5,5, si può calcolare che detto rapporto tra fosfati sodici abbia approssimativamente un valore 1/100 invece che circa 4 come nel sangue.
Un altro meccanismo posto in opera, sempre nel rene, per la conservazione degli ioni Na+ implica lo scambio di questi con gli ioni NH4+ (ioni ammonio) formatisi entro le cellule dei tubuli.
Link correlati:
Qual è la composizione del sangue?
Qual è il pH del caffè?
Qual è il pH di un sapone neutro?
Che cos'è l'emocateresi?
Qual è la percentuale dei gruppi sanguigni in Italia e nel resto del mondo?
Qual è il pH del latte?
Studia con noi