Nitrato di argento
Proprietà e caratteristiche del nitrato di argento. Vendita di nitrato di argento.
Il nitrato di argento è un sale ternario con formula chimica AgNO3.
Il nome IUPAC è: acido triossonitrato di argento.
È un sale molto solubile in acqua.
Si presenta come una polvere cristallina incolore che fonde a 212°C e si decompone al di sopra dei 400°C. Ha densità di 4,35 g/cm3 e una massa molare pari a 169,87 g/mol.
Il nitrato di argento si decompone facilmente alla luce e per tale motivo viene conservato in bottiglie di plastica scure.
Attenzione a non toccare il nitrato di argento con le mani
Toccando una soluzione di nitrato di argento si vede che, nelle ore successive, si viene a formare una intensa macchia di colore rosso/bruno.
Ciò è dovuto al fatto che il nitrato di argento, uno volta assorbito dalla pelle, viene a contatto con la luce solare e si decompone in argento che crea una macchia di questo colore. Come è possibile notare nell'immagine seguente le macchie possono essere anche molto vistose.

Macchia sulla pelle dovuta al nitrato di argento.
È per questo motivo che quando si adopera il nitrato di argento è buona norma usare i guanti monouso e il camice da laboratorio.
Se non sei stato previdente e hai le mani con le macchie nere dovute al nitrato di argento non ti ingegnare per trovare rimedio. Grazie al ricambio cellulare, nel giro di una settimana infatti le macchie spariranno da sole.
La sensibilità del nitrato di argento alla luce viene sfruttato in campo fotografico.
pH di una soluzione di nitrato di argento
AgNO3 disciolto in acqua si dissocia nei suoi due ioni:
AgNO3 → Ag+ + NO3−
Mentre lo ione NO3− non dà idrolisi, lo ione Ag+ dà idrolisi leggermente acida:
Ag+ + H2O → AgOH + H+
Pertanto il pH di una soluzione acquosa di AgNO3 è leggermente acido.
Si tenga conto che 100 g di AgNO3 disciolti in 1 L di acqua impartiscono all'acqua un pH ≈ 6,0.
Produzione del nitrato di argento
Il nitrato di argento viene ottenuto per azione dell'acido nitrico sull'argento metallico.
Dalla evaporazione della soluzione così ottenuta è possibile ottenere il nitrato di argento.

Nitrato di argento.
Impieghi
Il nitrato di argento viene impiegato per preparare la maggior parte dei composti dell'argento.
Importante è l'impiego del nitrato di argento nel processo di argentatura degli specchi. Per ottenere l'argentatura degli specchi si precipita l'argento da soluzioni di nitrato di argento e ammoniaca, per aggiunta di acido tartarico o di sale di Seignette (tartrato di sodio e potassio).
In chimica analitica (argentometria) AgNO3 viene impiegato per riconoscere e dosare gli alogeni.
La reazione tra nitrato di argento e ioduro di potassio viene invece utilizzata per produrre AgI, un importante composto in campo fotografico.
AgNO3(aq) + KI(aq)→ AgI(s) + KNO3(aq)
AgNO3 trova impiego anche grazie alle sue proprietà cauterizzanti e disinfettanti.
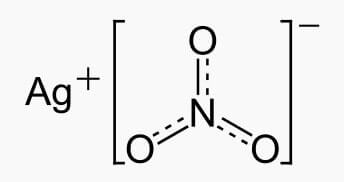
Struttura del nitrato di argento, AgNO3
Ioni equivalenti: Ag+ , NO3−
Link correlati:
Breve storia della fotografia
Proprietà, caratteristiche e formula del nitrato piomboso
Studia con noi