Ipoazotide
Proprietà e caratteristiche dell'ipoazotide
L'ipoazotide è un composto con formula chimica NO2.
Indicato anche con i nomi di anidride nitroso-nitrica o diossido di azoto l'NO2 è una specie gassosa con temperatura critica pari a 157,8°C, che a pressione atmosferica condensa a 21,2°C e solidifica a -11,20 °C.
NO2 è il più tossico fra gli ossidi dell'azoto che inquinano l'atmosfera (proviene da processi industriali e si forma dai gas di scappamento dei veicoli). 5 parti per milione (p.p.m.) sono già causa di infiammazione alle vie respiratorie; alte concentrazioni (>100 p.p.m.) divengono letali per prolungata aspirazione.
La molecola NO2, come la molecola dell'ossido di azoto NO contiene un elettrone dispari ed è quindi paramagnetica; essa risuona fra più forme:
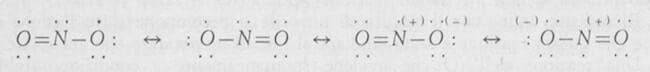
L'energia di risonanza impegna l'elettrone dispari della molecola meno di quanto non avvenga nella molecola dell'NO, e pertanto NO2 è più reattivo di NO ed ha tendenza a dimerizzare:
2 NO2 → N2O4 + 58,6 kJ
La molecola NO2 è colorata in rosso bruno ed è paramagnetica; il dimero N2O4 (molecola planare O2N-NO2) è incolore e diamagnetico.
La molecola NO2 perde facilmente il suo elettrone dispari (energia di ionizzazione = Ei =10 eV), formando lo ione nitronio NO2+.
Preparazione della ipoazotide
L'ipoazotide può prepararsi oltre che per ossidazione di NO con ossigeno, anche per riduzione di acido nitrico concentrato (si veda oltre) o per decomposizione termica dei nitrati di alcuni metalli pesanti.
Ad esempio:
2 Pb(NO3)2 → 2 PbO + 4 NO2↑ + O2↑
Il diossido di azoto si scioglie in acqua e nelle soluzioni acquose alcaline, disproporzionandosi nel primo caso in acido nitroso (HNO2 acido debole) ed in acido nitrico (HNO3, acido forte) e nel secondo negli ioni nitrito (NO2−) e nitrato (NO3−):
N2O4 + 2 H2O → HNO2 + H3O+ + NO3−
N2O4 + 2 OH− → NO2− + NO3− + H2O
È a queste reazioni di disproporzione che N2O4 deve il suo nome tradizionale di anidride nitrosa-nitrica.
Ipoazotide da riduzione di acido nitrico
Come detto, l'ipoazotide può prepararsi per riduzione di acido nitrico concentrato.
Nel video seguente, all'interno del becher due cilindretti di rame vengono fatti reagire con acido nitrico HNO3 concentrato.
Dalla reazione chimica che ne scaturisce si ottiene una soluzione colorata di nitrato rameico Cu(NO3)2 e vapori bruni, più pesanti dell'aria, di anidride nitrosa (NO2) secondo la reazione:
Cu + 4 HNO3 → Cu(NO3)2 + 2 NO2 (g) + 2 H2O
I vapori bruni di ipoazotide si "depositano" sul banco di lavoro proprio perché più pesanti dell'aria.
Studia con noi