Anidride nitrica
Proprietà e caratteristiche dell'anidride nitrica
L'anidride nitrica, nota anche con il nome di pentossido di diazoto, è un composto con formula chimica N2O5 (O2N-O-NO2).
Presenta la seguente struttura:
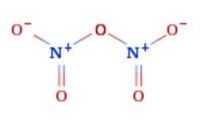
È un solido incolore, termodinamicamente instabile (ΔG° = 113,8 kJ/mol), che fonde a 30°C e bolle a 47°C, decomponendosi in ossigeno ed ossidi inferiori di azoto, secondo la reazione:
2 N2O5 → O2 + 4 NO2
Ha densità pari a 2,05 g/cm3 e massa molare di 108,01 g/mol.
Preparazione dell'anidride nitrica
È possibile preparare l'anidride nitrica disidratando acido nitrico concentrato con pentossido di difosforo (anidride fosforica) che forma acido metafosforico:
2 HNO3 + P2O5 → N2O5 + 2 HPO3
Alternativamente è possibile preparare l'anidride nitrica ossidando NO2 con ozono:
2 NO2 + O3 → N2O5 + O2
Reazioni caratteristiche dell'anidride nitrica
L'anidride nitrica N2O5 reagisce con acqua formando acido nitrico:
N2O5 + H2O → 2 HNO3
da cui il suo nome tradizionale di anidride nitrica.
N2O5 si comporta da forte ossidante nei confronti di metalli, non metalli e sostanze organiche.
Ai raggi X i cristalli N2O3 mostrano una struttura ionica NO2+NO3−, e quindi N2O5 può considerarsi come nitrato (NO3−) di nitronio (NO2+).
L'anidride nitrica e le piogge acide
Le attività industriali, il riscaldamento degli edifici e l'utilizzo degli autoveicoli sono responsabili dell'inquinamento atmosferico in seguito all'emissione (anche e non solo) di grandi quantità di ossidi di azoto (genericamente definiti NOx).
Questi gas, in seguito a reazioni chimiche catalizzate dalla luce solare, si ossidano ad anidride nitrica N2O5, la quale, a contatto con l'acqua piovana, produce acido nitrico HNO3, sostanza responsabile dell'aumento dell'acidità delle precipitazioni atmosferiche (piogge acide).
Studia con noi