Trizio
Che cos'è il trizio?
Il trizio, noto anche come tritio o idrogeno-3 è un isotopo radioattivo dell'idrogeno; viene rappresentato con il simbolo 3H o con il simbolo T.
È un nuclide con numero atomico Z = 1 e numero di massa A = 3, pertanto è formato da un protone, un elettrone e due neutroni.
Protone e neutroni formano il nucleo dell'atomo, mentre l'elettrone gravita attorno al nucleo atomico secondo lo schema semplificato di seguito rappresentato:
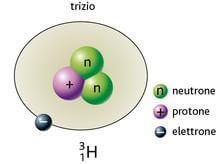
Il nucleo atomico del trizio è detto tritone o trizione.
In condizioni standard di pressione e di temperatura il trizio si presenta come molecola biatomica T2.
Essendo radioattivo, decade - tramite emissione β - formando elio-3 (3He):
3T → 3He + e− + neutrino elettronico
La radiazione β emessa dal decadimento del trizio ha una energia di 19 KeV.
Il nuclide in questione viene impiegato come tracciante in ricerche chimiche e biochimiche ed è un componente della bomba termonucleare o a idrogeno.
Preparazione del trizio
Il trizio fu prodotto per la prima volta bombardando composti di deuterio con deutoni a elevata energia. La reazione nucleare può essere scritta nel seguente modo:
2H + 2H → 3H + 1H
Un gran numero di reazioni nucleari simili portano al trizio. La più importante di queste è l'assorbimento di neutroni lenti dall'isotopo del litio di numero di massa 6 secondo l'equazione:
6Li + n → 3H + 4He
Presenza in natura del trizio
Nonostante sia radioattivo e abbia una emivita breve, il trizio è presente, seppure in modeste quantità, in natura.
Ciò è dovuto al fatto che nell'alta atmosfera il trizio viene continuamente prodotto secondo la reazione:
14N + n → 3H + 12C
Dopo la sua produzione nell'alta atmosfera il trizio entra a far parte del ciclo geochimico dell'acqua.
Nel 1949 fu misurata la quantità di trizio prodotto dalla radiazione cosmica valutandola a 30 atomi per cm2 per minuto.
Le successive esplosioni termonucleari portarono il contenuto in trizio dell'atmosfera a valori circa 10 volte superiori a quelli precedenti, introducendo così nel ciclo dell'acqua in tutto il mondo un tracciante artificiale.
Dal 1962, dopo la cessazione degli esperimenti termonucleari, questa quantità artificialmente prodotta va decadendo con un tempo di dimezzamento di 12,33 anni.
Con una emivita così breve è chiaro che questo radionuclide è di notevole interesse per la meteorologia, l'oceanografia, così come per studi di movimenti di masse di acque e sorgenti, mentre non ha alcun interesse per le misure di età.
Link correlati:
Quanti e quali sono gli isotopi dell'idrogeno?
Che cos'è il Curie come unità di radioattività?
Qual è il simbolo del numero atomico?
Che cos'è e quanto vale un becquerel?
Studia con noi