Densità del ghiaccio
Quanto vale la densità del ghiaccio?
Volete sapere quanto vale la densità del ghiaccio?
Ve lo diciamo subito.
Alla temperatura di 0°C e alla pressione di 1 atm, la densità del ghiaccio è pari a 916,8 kg/m3.
kg/m3 è l'unità di misura della densità.
Ciò significa che, alla temperatura di 0°C, 1 m3 di ghiaccio ha una massa di 916,8 kg.
Essendo la densità del ghiaccio (916,8 kg/m3) inferiore alla densità dell'acqua (999,8 kg/m3), si ha che il ghiaccio galleggia sull'acqua.
Questo fenomeno, seppur deleterio per le tubazioni dell'acqua nei mesi invernali (il ghiaccio aumenta di volume e rompe le tubature), è fondamentale per la continuazione della vita negli ambienti acquatici: lo strato di ghiaccio che si forma sulle superfici di laghi, stagni, etc... non va ad accumularsi sul fondo, bensì galleggia (proprio perché di densità inferiore a quella del liquido) isolando termicamente l'acqua liquida sottostante e proteggendo gli organismi acquatici che vi si trovano.
La densità del ghiaccio in kg/dm3 e g/cm3
Volendo esprimere la densità del ghiaccio in kg/dm3 o in g/cm3, si ha che:
916,8 kg/m3 = 916,8 kg / (1000 dm3) = 0,9168 kg / dm3
0,9168 kg / dm3 = 0,9168 · (1000 g) / (1000 cm3) = 0,9168 g/cm3
Comportamento anomalo della densità del ghiaccio
Passando dallo stato solido (d = 0,9168 g/cm3) allo stato liquido (d = 0,9998 g/cm3) la densità dell'acqua aumenta.
Solidi che fondendo aumentano di densità sono assai rari e pertanto l'acqua ha un comportamento anomalo.
Il motivo di tale anomalia è da ricercarsi nella formazione dei legami a idrogeno. Ciascuna molecola di H2O allo stato solido può formare infatti 4 legami a idrogeno con altre 4 molecole H2O dando vita ad una struttura tetraedrica, che è una struttura aperta.
I legami a idrogeno sono legami chimici direzionali e per loro stessa natura tendono ad allontanare le molecole di acqua.
Nella fusione del ghiaccio una elevata percentuale di legami idrogeno vengono rotti (circa il 20-30%).
Nella rottura dei legami a idrogeno, le molecole di H2O possono impacchettarsi in modo più compatto, e di conseguenza si ha una diminuzione di volume e quindi un aumento di densità (si ricordi che d = m / V).
Riassumendo
l legame a idrogeno spiega il motivo per cui la densità del ghiaccio è inferiore a quella dell'acqua.
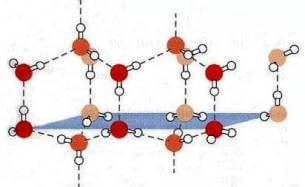
Infatti quando l'acqua congela le molecole sono costrette a distanziarsi per formare la struttura esagonale ordinata tipica del ghiaccio meno densa della struttura disordinata tipica dell'acqua allo stato liquido:
Link correlati:
Quanto vale la densità dell'acqua di mare?
Quanto vale la densità dell'anidride carbonica?
Quanto vale la densità dell'acqua?
Perché il ghiaccio galleggia sull'acqua?
Quanto vale la densità dell'elio?
Quanto vale la densità dell'idrogeno?
Quanto vale la densità dell'olio?
Quanto vale la densità della sabbia?
Studia con noi