Studio della coordinata di reazione
Esercizio sullo studio della coordinata di reazione di una generica reazione chimica
Viene rappresentato il diagramma di reazione per una generica reazione chimica A + B → C.
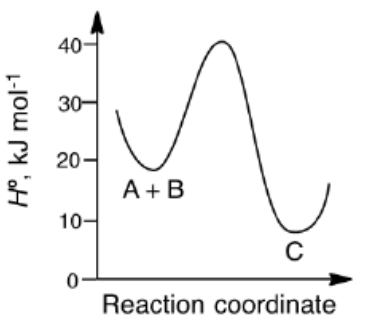
Si stabilisca se la reazione è esotermica o endotermica e a quanti kJ/mol corrisponde il valore dell'energia di attivazione Ea.
Svolgimento dell'esercizio
La coordinata di reazione è un grafico che mostra l'evoluzione di una reazione chimica in funzione di un dato "cammino di reazione"; nel nostro caso, che è anche quello più frequente, la coordinata di reazione mostra l'andamento dell'entalpia (misurata in kJ/mol) associata alla reazione.
A e B sono due generici reagenti di una reazione, mentre C è l'unico generico prodotto della reazione chimica.
Fatta questa breve ma necessaria introduzione, rispondiamo alla prima domanda che ci viene posta e stabiliamo se la reazione è esotermica oppure endotermica.
Una reazione si dice esotermica se cede calore all'ambiente; viceversa, una reazione si dice endotermica se acquista calore dall'ambiente.
In una reazione chimica esotermica il valore dell'entalpia diminuisce, pertanto l'entalpia dei prodotti è inferiore a quella dei reagenti; in una reazione chimica endotermica, invece, il valore dell'entalpia aumenta, pertanto l'entalpia dei prodotti è superiore a quella dei reagenti.
Come è possibile notare dal grafico il valore dell'entalpia di C è inferiore all'entalpia di A+B quindi la reazione rappresentata è esotermica.
Rispondiamo ora alla seconda domanda e ci chiediamo quanto vale il valore dell'energia di attivazione Ea.
L'energia di attivazione è l'energia minima necessaria ad un sistema per innescare una reazione chimica e corrisponde alla differenza tra il valore dell'energia del complesso attivato e il valore dell'energia dei reagenti.
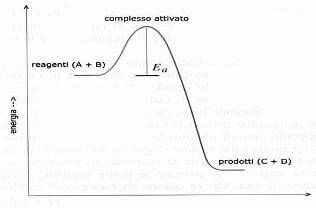
Possedere una energia pari o superiore al valore dell'energia di attivazione, consente alle molecole dei reagenti - che collidono tra loro - di formare il complesso attivato.
Nel nostro caso il valore dell'energia del complesso attivato vale 40 kJ/mol, mentre il valore dell'energia dei reagenti vale 20 kJ/mol (si veda il grafico del testo dell'esercizio). Pertanto l'energia di attivazione vale: Ea = 40 - 20 = 20 kJ/mol.
Link correlati:
Calcolo dell'età di un campione tramite l'analisi al carbonio-14
Esercizio svolto su una reazione del secondo ordine
Esercizio sulla reazione di inversione del saccarosio
Esercizio sull'ordine di reazione e la costante specifica di velocità
Studia con noi