Temperatura critica dell'acqua
Che cos'è la temperatura critica dell'acqua?
Se si riscalda una determinata quantità di acqua allo stato liquido contenuta in un tubo di Natterer (capillare saldato di quarzo ed a pareti assai spesse), giunti alla temperatura di 374,1°C (temperatura critica dell'acqua) scompare la separazione fra liquido e vapore e all'interno del capillare si ha un'unica fase detta fase critica.
La pressione corrispondente alla temperatura di 374,1°C è detta pressione critica dell'acqua e vale 218,3 atm.
La temperatura di 374,1°C e la pressione di 218,3 atm vengono perciò a costituire una coppia univoca di valori al di sopra della quale l'acqua non esiste più come miscela bifase vapore-liquido ma esiste in un'unica fase detta fase critica.
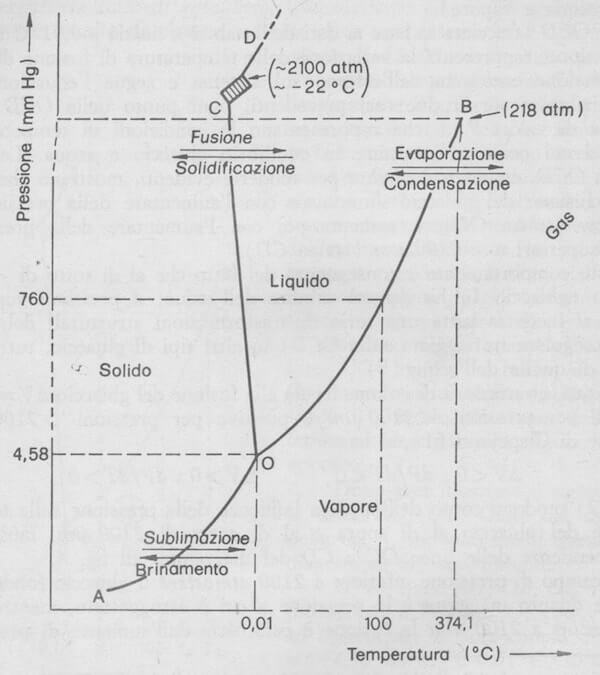
Dallo studio del diagramma di stato dell'acqua è facile individuare la temperatura critica dell'acqua.
Il tratto di curva OB rappresenta la variazione della pressione di vapore dell'acqua con la temperatura e definisce i valori di T e di P ai quali esiste un equilibrio del sistema liquido-vapore
Si nota che tale tratto di curva non si estende indefinitivamente ma si interrompe in un determinato punto (B) al quale corrisponde un vapore di temperatura di 374,1°C.
Ciò esprime ed evidenzia il fatto che al di sopra di tale temperatura la fase liquida e la fase vapore dell'acqua diventano indistinguibili.
Temperatura critica dell'acqua (374,1°C), pressione critica dell'acqua (218,3 atm) e densità critica dell'acqua (cioè densità della fase critica = 0,400 g/cm3) determinano il punto critico dell'acqua.
Link correlati:
Che cos'è un diagramma di stato?
Studia con noi