Tavola periodica
La tavola periodica degli elementi chimici
In questa lezione vedremo che cos'è la tavola periodica degli elementi chimici e come è strutturata; studieremo che cosa sono i gruppi e che cosa sono i periodi.
Vedremo a quale illustre chimico russo si deve la scoperta della tavola periodica e come sono sistemati e quali proprietà hanno gli elementi chimici della tabella.
Nella seconda metà del XIX secolo la scoperta di nuovi elementi e lo studio delle loro proprietà, sia fisiche sia chimiche, evidenziarono alcune analogie nelle proprietà di certi gruppi di essi.
Vi furono quindi parecchi tentativi per classificare gli elementi in accordo con le analogie osservate; il maggior risultato, in questa attività di sintesi, venne ottenuto dal chimico russo Dmitrij Ivanovič Mendeleev (Tobol'sk, 8 febbraio 1834 – San Pietroburgo, 2 febbraio 1907) che, nel 1869, propose la sua tavola periodica degli elementi.
In essa gli elementi sono ordinati in accordo con le loro proprietà più evidenti, in particolare il peso atomico e la valenza (ossia un "valore" che indica il numero di atomi di idrogeno che si possono combinare con un atomo dell'elemento considerato).
I posti lasciati inizialmente vuoti poiché di elementi non ancora scoperti, furono successivamente riempiti; parliamo del gallio e del germanio. Di essi il chimico russo predisse le proprietà chimiche che, secondo le sue attese, dovevano avere in base alla posizione occupata nella tabella.
Quindi fu possibile prevedere e successivamente verificare caratteristiche fisiche e chimiche di elementi rari in natura, tramite la conoscenza delle proprietà degli elementi adiacenti.
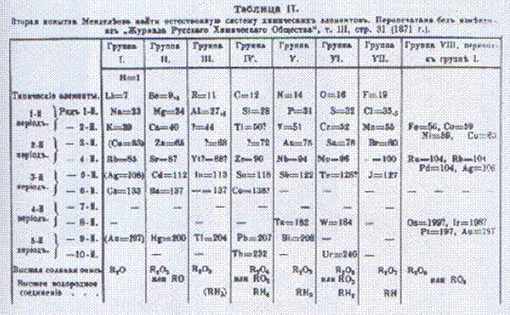
La tavola periodica di Mendeleev.
Solo per quattro coppie di elementi l'ordine assegnato nella tavola differiva dal numero atomico crescente; solo successivamente si capì che, in realtà, gli elementi chimici dovevano essere ordinati per numero atomico crescente* (e non per peso atomico).
* il numero atomico (indicato con la lettera Z) indica il numero di protoni presenti nel nucleo di un atomo.
La moderna tavola periodica degli elementi
Nella moderna tavola periodica degli elementi, a differenza di quanto previsto nella tavola periodica di Mendeleev, gli elementi chimici sono ordinati in base al numero atomico crescente.
La caratteristica fondamentale di questa tabella è la periodica distribuzione degli elettroni nel livello più esterno.
Per esempio, se confrontiamo le configurazioni elettroniche di litio, sodio e potassio, notiamo che tutte quante hanno un solo elettrone nel livello più esterno (sottolivello s).
Analogamente, confrontando le configurazioni elettroniche dei gas nobili notiamo che tutte quante terminano nello stesso identico modo (s2p6).
Pertanto, gli elementi della stessa colonna (gruppo) hanno configurazione elettronica esterna simile e ciò comporta la somiglianza delle proprietà chimiche e delle proprietà fisiche di questi elementi.
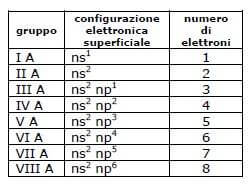
La periodicità della tavola degli elementi è quindi dovuta alla struttura elettronica più esterna degli elementi. Gli elettroni presenti nell'ultimo livello di energia sono chiamati elettroni di valenza.
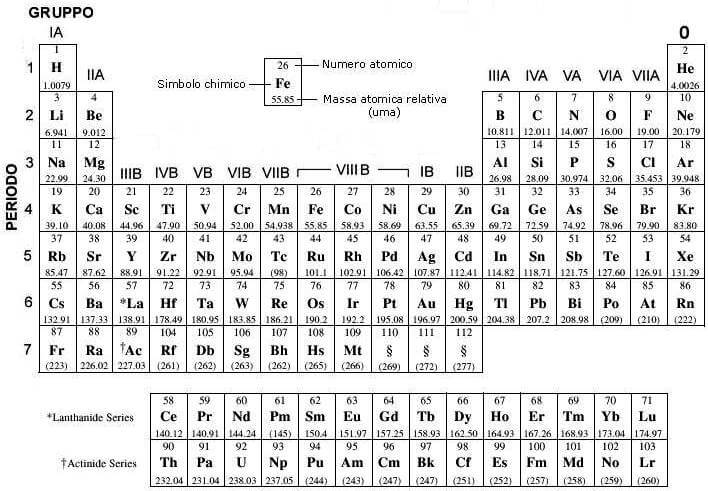
Le caratteristiche principali della tavola periodica sono:
1) Gli elementi sono ordinati in funzione del numero atomico crescente; il numero atomico (indicato con la lettera Z) indica il numero di protoni presenti nel nucleo dell'atomo.
2) Nella tavola periodica sono presenti 7 righe orizzontali cioè 7 periodi. Il periodo di un elemento indica il livello di energia sul quale sono collocati gli elettroni di valenza. Per esempio, gli elementi appartenenti al 3° periodo (Na, Mg, Al, ... Ar) hanno gli elettroni di valenza sul terzo livello di energia.
3) Nella tavola periodica sono presenti 18 righe verticali cioè 18 gruppi. I gruppi della tavola periodica hanno una doppia numerazione: la prima in numeri arabi da 1 a 18; la seconda, molto più importante, in numeri romani da I a VIII. Quest'ultima interessa soltanto quei gruppi in cui gli elettroni stanno riempendo i sottolivelli s e p.
Al numero romano corrisponde il numero di elettroni di valenza: così, H, Na, K, Rb, ecc. hanno tutti un solo elettrone di valenza; viceversa Ne, Ar, Kr, Xe, ecc. hanno tutti otto elettroni di valenza (l'unica eccezione è costituita dall'elio che, anche se posizionato nell'VIII gruppo ha solo due elettroni di valenza).

4) Fra il gruppo II e il gruppo III si trovano gli elementi di transizione nei quali si stanno riempendo i sottolivelli di tipo d e che occupano la zona centrale della tavola periodica.
Tali elementi sono raggruppati in tre serie:
- la prima serie va dallo scandio (numero atomico 21) allo zinco (numero atomico 30);
- la seconda serie va dall'ittrio (numero atomico 39) al cadmio (numero atomico 48);
- la terza serie va dal lantanio (numero atomico 57) al mercurio(numero atomico 80).
5) In fondo alla tavola periodica ci sono i lantanidi e gli attinidi. In questi elementi, che sono 28, si stanno riempendo i sottolivelli di tipo f.
I lantanidi (o lantanoidi), sono un gruppo di 14 elementi chimici aventi numero atomico compreso tra 58 e 71; tutti questi elementi hanno proprietà chimiche simili a quelle del lantanio, elemento da cui prendono il nome.
Gli attinidi (o attinoidi), sono un gruppo di 14 elementi chimici aventi numero atomico compreso tra 90 e 103; tutti questi elementi hanno proprietà chimiche simili a quelle dell'attinio, elemento da cui prendono il nome.
Link correlati:
Vuoi sapere quanti sono gli elementi della tavola periodica?
Ti serve una tavola periodica con numeri di ossidazione?
Tavola periodica completa di tutte le proprietà degli elementi chimici
Tavola periodica con configurazione elettronica di tutti gli elementi chimici
Elenco alfabetico e per numero atomico degli elementi chimici
Studia con noi