Elettrodo a vetro
Determinazione del pH tramite elettrodo a vetro
La misura del pH con l'elettrodo di idrogeno nel passato ha rappresentato l'unico mezzo per misurare con esattezza il pH di una soluzione.
Successivamente si è però affermato un altro elettrodo più versatile nell'uso, che oggi è universalmente impiegato: l'elettrodo a vetro.
Tale elettrodo, la cui comparsa sul mercato risale attorno al 1935, è assai poco soggetto ad avvelenamento (al contrario del platino platinato dell'elettrodo di idrogeno), non è influenzato dalla presenza di ossidanti o di riducenti nella soluzione, funziona bene anche in mezzi non acquosi ed ha risposta assai rapida.
Funzionamento dell'elettrodo a vetro
Il funzionamento dell'elettrodo a vetro è basato sulla proprietà di certe membrane di vetro (composte indicativamente dal 72% di SiO2, dal 22% di Na2O e dal 6% di CaO) di scambiare ioni Na+, dei silicati che costituiscono il vetro stesso, con ioni idrogeno (e solo con questi) presenti nella soluzione con cui sono a contatto.
La misura del pH con l'elettrodo di vetro si esegue mediante costruzione di una pila del tipo:
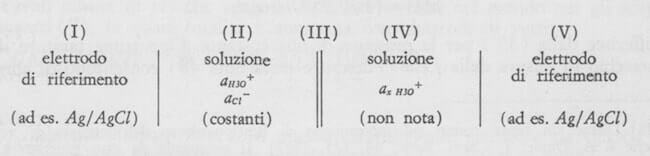
ove:
- I e V sono di norma due elettrodi a calomelano o a cloruro d'argento;
- II è una soluzione tampone contenente anche ioni necessari al funzionamento dell'elettrodo di riferimento I immerso in essa;
- III è la membrana di vetro;
- IV la soluzione di cui si vuole misurare il pH.
La realizzazione sperimentale della pila è schematizzata nella figura seguente:
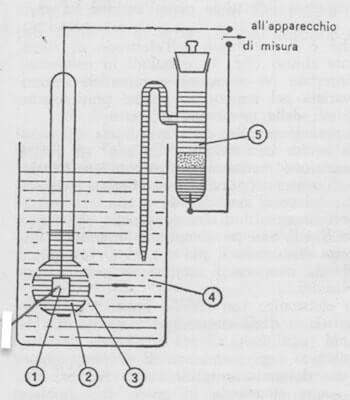
1-semilelemento di riferimento interno all'elettrodo di vetro; 2-soluzione tampone interna all'elettrodo di vetro; 3-membrana di vetro generatrice della f.e.m. della pila; 4-soluzione di cui si vuole misurare il pH; 5-semielemento di riferimento esterno.
La vera pila, cioè il sistema che genera la f.e.m., è costituita dalla membrana di vetro a contatto con le due soluzioni a diverso pH; i due elettrodi di riferimento fungono da sonde elettriche, che hanno soltanto il compito di portare allo strumento di misura la f.e.m. che si genera fra le due facce della membrana a contatto con le soluzioni.
Tra valore del pH incognito e f.e.m. della pila esiste la relazione:
pH = (E/0,059) + cost
Opportune tarature dell'apparecchio di misura della f.e.m. consentono di annullare il valore della costante.
Meccanismo di funzionamento dell'elettrodo a vetro
Il potenziale generato dall'elettrodo a vetro è la somma di più potenziali in serie:
- il potenziale (E1) dell'elettrodo di riferimento interno;
- il potenziale (E2) che si genera nell'interfase fra soluzione e superficie interna della membrana di vetro;
- il potenziale di asimmetria (E3) della membrana di vetro, dovuto alle inevitabili disomogeneità strutturali di questa;
- il potenziale (E4) che si genera all'interfase fra superficie esterna della membrana di vetro e soluzione di cui si effettua la misura del pH.
I potenziali E2 ed E4 sono generati dallo scambio ionico fra ioni Na+ presenti nelle superfici di vetro e ioni H+ presenti come ioni idronio nelle soluzioni; lo scambio è reso possibile dalle piccole dimensioni dello ione H+ e facilitato dal fatto che molecole H2O delle soluzioni penetrano nelle superficie della membrana di vetro per alcuni strati molecolari di questa; rendono così meno discontinuo il campo elettrico interfasale e diminuiscono la resistenza della membrana (gli elettrodi di vetro vanno mantenuti immersi in acqua anche quando non vengono usati, proprio per evitare che la loro superficie esterna perda quest'acqua di absorbimento.
I potenziali E1 , E2 , E3 sono costanti: E1 perché è il potenziale dell'elettrodo di riferimento contenuto in un bulbo di vetro ermeticamente chiuso e quindi in condizioni invariabili nel tempo; E2 perché la struttura dell'interfase fra soluzione e superficie interna della membrana di vetro si mantiene anch'essa invariata nel tempo; E3 perché praticamente invariate si mantengono anche le asimmetrie strutturali della membrana di vetro.
Il potenziale E4, potenziale all'interfase fra superficie esterna della membrana di vetro e soluzione di cui si vuol determinare il pH, varia invece in funzione della concentrazione di ioni H+ di questa secondo la relazione vista in precedenza: pH = (E/0,059) + cost.
Taratura dell'elettrodo a vetro
Per misurare il pH di una soluzione mediante elettrodo di vetro, occorre prima effettuare la taratura dello strumento di misura (piaccametro).
Questa consiste essenzialmente nella misura del pH di una soluzione tampone assai stabile e con pH esattamente noto (tampone di taratura).
Agendo su opportuni circuiti di compensazione che fanno parte del piaccametro, si annulla il potenziale E = E1 + E2 + E3 e si porta l'apparecchio a segnare l'esatto valore del pH del tampone di taratura.
A questo punto il pHmetro è pronto per misure di pH su altre soluzioni.
Sullo stesso schema di funzionamento si costruiscono oggi membrane di diverse, opportune composizioni, in grado di scambiare ciascuna una determinata specie ionica (ad esempio Li+, Na+, K+, Rb+, Cs+, Ca2+, ecc).
Studia con noi