Produzione acido solforico
Metodi di produzione industriale dell'acido solforico
La produzione industriale dell'acido solforico avviene attraverso due processi diversi:
1) metodo delle camere di piombo, che produce acido solforico di media concentrazione, metodo ormai quasi completamente abbandonato;
2) metodo catalitico o di contatto, che produce acido solforico concentrato e acido solforico fumante.
Fino ai primi anni del 1900 tutto l'acido solforico veniva prodotto con il metodo delle camere di piombo. In seguito i vecchi impianti a camere di piombo furono gradatamente sostituiti dai moderni impianti di catalisi ed attualmente, fatta eccezione per qualche vecchio impianto ancora funzionante, tutto l'acido solforico viene prodotto col processo catalitico.
Ambedue i processi ottengono l'acido solforico attraverso le seguenti tre fasi:
1) Preparazione della SO2 e sua purificazione;
2) Ossidazione catalitica della SO2 a SO3;
3) Idratazione della SO3 e sua trasformazione in acido solforico.
Produzione dell'acido solforico: processo catalitico
Il processo catalitico realizza la ossidazione della SO2 a SO3 mediante l'ossigeno atmosferico secondo la seguente reazione di equilibrio:
2 SO2 + O2 ⇄ 2 SO3
L'equilibrio di questa reazione ad alta temperatura è praticamente spostato verso destra ma è indispensabile la presenza di un catalizzatore.
Nel passato venivano usati dei catalizzatori a base di platino, molto costosi. Oggi si usano con successo catalizzatori a base di anidride vanadica V2O5 alla temperatura di 400-450°C alla quale il rendimento della reazione è praticamente del 100%.
L'anidride solforosa impiegata in questo processo deve avere un elevato grado di purezza; in altri termini deve essere esente da sostanze capaci di avvelenare il catalizzatore (specialmente As2O3 e SeO2 particolarmente nocivi).
Per tale motivo i gas solforosi, prima di essere inviati alla torre di catalisi devono essere sottoposti ad un accurato procedimento di purificazione e ove è possibile anziché essere prodotti mediante arrostimento delle piriti (che contengono sempre tracce di arsenico e di selenio) sono prodotti per combustione diretta dello zolfo che fornisce SO2 molto pura.
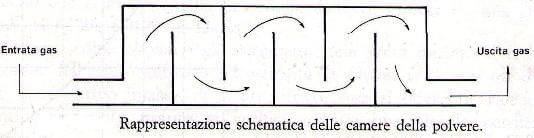
Previamente depurato dal pulviscolo grossolano attraverso le camere della polvere e successivamente con elettrofiltri, i gas entrano in una torre di lavaggio dove incontrano una corrente di acqua che ne asporta le impurezze residue.
Nel corso dell'operazione di lavaggio il gas si satura di umidità la quale deve essere eliminata perché nociva alla reazione di catalisi. A tale scopo i gas provenienti dalla torre di lavaggio si fanno passare in una torre di essiccamento dall'alto della quale cade una pioggia di acido solforico concentrato (al 100% di H2SO4) che essendo avidissimo di acqua trattiene tutta l'umidità in essi presente.
Il volume dell'acido di lavaggio è calcolato in modo che esso si diluisca fino ad un titolo del 90% di H2SO4, a spese dell'umidità sottratta ai gas.
Questo acido che si raccoglie alla base della torre di essiccamento viene convogliato alla torre di assorbimento.
Dalla torre di essiccamento il gas solforoso puro e secco entra nella torre di catalisi nella quale avviene la conversionedella anidride solforosa in anidride solforica secondo la seguente reazione:
2 SO2 + O2 ⇄ 2 SO3
La torre di catalisi è costituita da una serie di ripiani sui quali è sistemato il catalizzatore finamente suddiviso. Esso è generalmente costituito da anidride vanadica V2O5.
Dalla torre di catalisi, i gas contenenti la SO3 passano in una torre di assorbimento dall'alto della quale cade una pioggia di acido solforico al 90% (quello stesso acido che scarica la precedente torre di essiccamento) che cede alla SO3 l'acqua che aveva assorbito. In questo modo l'anidride SO3 viene convertita in H2SO4.
SO3 + H2O ⇄ H2SO4
Il volume della SO3 che si fa circolare nella torre e il volume dell'acido di colaggio sono calcolati in modo che all'uscita dalla torre di assorbimento si abbia un acido al 100% di H2SO4 denominato acido solforico monoidrato. Di questo acido, una parte ritorna alla sommità della torre di essiccamento e la parte rimanente và al consumo.
Studia con noi