Fullerene
La terza forma allotropica del carbonio: il fullerene
Il fullerene, noto anche con il nome di buckminsterfullerene è un composto a struttura poliedrica-sferoidale a 60 atomi di carbonio.
Viene così chiamato perché la sua forma ricorda quella delle cupole geodetiche ideate dall'architetto e designer statunitense R. B. Fuller.
Nel fullerene ciascun atomo di carbonio è ibridato sp2 (per info: ibridazione sp2) e nel suo complesso la struttura ha la forma di un icosaedro tronco.
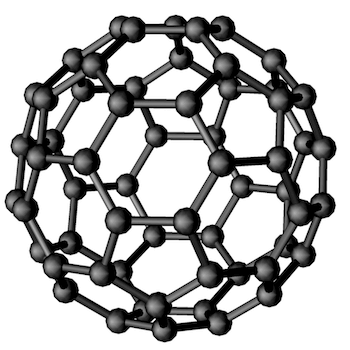
Struttura icosaedro tronca del fullerene (C60).
La struttura è quindi formata da 32 facce (di cui 12 pentagonali e 20 esagonali), 90 spigoli e 60 vertici.
Storia del fullerene
Ipotizzato già nel 1970, il C60 fu sintetizzato per la prima volta nel 1986, in miscela con altri fullereni, da H. Kroto, R. Smalley e R. Curi.
Grazie a tale scoperta - nel 1996 - i tre scienziati furono insigniti del premio Nobel per la chimica.
Il sorprendente risultato fu ottenuto con la tecnica dell'ablazione laser di una superficie di grafite con la quale si dovevano riprodurre condizioni simili a quelle che avrebbero generato molecole lineari organiche nello spazio interstellare.
Proprietà del fullerene
Il buckminsterfullerene (o fullerene) si presenta come un solido nero cristallino stabile fino a 400°C.
Questo fullerene è per sua natura un isolante ma diventa conduttore e superconduttore a basse temperature quando, tramite drogaggio, ingloba un
metallo alcalino.
Ad esempio, il composto K3C60 è superconduttore a 19 K.
Sono stati preparati svariati polimeri contenenti l'aggregato C60 e diversi metallofullereni o fulleruri; questi ultimi risultano ottimi superconduttori anche ad alte temperature.
Studia con noi