A quale pH inizia e termina la precipitazione dell'idrossido ferroso
Calcolo del pH al quale inizia e termina la precipitazione dell'idrossido ferroso
Partendo da una soluzione 0,032 mol/L di ioni Fe2+, a quale pH inizia a precipitare l'idrossido ferroso Fe(OH)2? A quale pH sarà completa al 99,99%?
Si sappia che per il Fe(OH)2 vale Kps = 8 · 10-16.
Svolgimento dell'esercizio
L'esercizio propone il calcolo del pH al quale inizia la precipitazione di Fe(OH)2 partendo da una soluzione 0,032 M di ioni Fe2+.
L'idrossido ferroso Fe(OH)2 si dissocia in acqua nel seguente modo:
Fe(OH)2 ⇆ Fe2+ + 2 OH−
Il prodotto di solubilità è dato dalla seguente relazione matematica:
Kps = [Fe2+] · [OH−]2
Ma la concentrazione degli ioni Fe2+ è nota e vale 0,032 mol/L. Ricaviamo dalla formula precedente il valore di [OH−]:
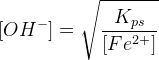
In cui:
- Kps = 8 · 10-16
- [Fe2+] = 0,032 M
Sostituendo i dati a disposizione si ha che:
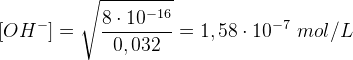
Pertanto nel momento stesso che inizia la precipitazione dell'idrossido ferroso la concentrazione degli ioni OH− è pari a 1,58 · 10-7 mol/L.
Non ci rimane altro che calcolare il pOH e quindi il pH. Il pOH è il logaritmo negativo in base 10 della concentrazione degli ioni OH−; in formula:
pOH = - log[OH−] = - log (1,58 · 10-7) = 6,80
Ricordando infine che pH + pOH = 14, si ha che:
pH = 14 - pOH = 14 - 6,80 = 7,20
Pertanto il pH a cui inizia a precipitare Fe(OH)2 da una soluzione 0,032 mol/L di ioni Fe2+ è pari a 7,20.
Determiniamo ora a quale pH termina la precipitazione di Fe(OH)2
Il testo dell'esercizio chiede di calcolare a quale pH sarà completa al 99,99% la precipitazione dell'idrossido in questione.
Se la precipitazione è completa al 99,99% significa che lo 0,01% di ioni Fe2+ è ancora in soluzione. Ciò equivale ad una concentrazione pari a:
[Fe2+] = 0,032 · 0,01 / 100 = 3,2 · 10-6 mol/L
Sostituendo questo dato nella formula:
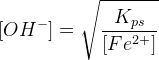
si ha che:
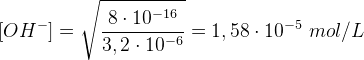
Da cui:
pOH = - log[OH−]= - log(1,58 · 10-5) = 4,80
e:
pH = 14 - 4,80 = 9,20
Studia con noi