Celle elettrolitiche
Che cosa sono le celle elettrolitiche?
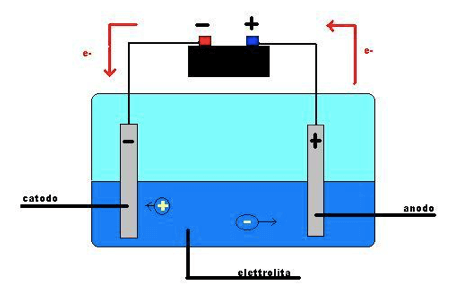
Una cella elettrolitica è un apparato costituito da un generatore di tensione i cui due poli sono chiusi in un circuito attraverso due elettrodi non a diretto contatto tra di loro ma immersi in un liquido.
Se il liquido è conduttore allora il circuito risulterà chiuso con passaggio di corrente tra i poli della batteria, altrimenti il circuito sarà aperto senza passaggio di corrente elettrica.
L'elettrodo connesso al polo negativo prende il nome di catodo mentre quello collegato al polo positivo si dice anodo. L'acqua pura non è conduttrice ma isolante.
Se nell'acqua si sciolgono sali o acidi essa diventa conduttrice. Tali sostanze disciolte nell'acqua che permettono la conduzione elettrica si dicono elettroliti.
L'acqua e la conducibilità elettrica
Abbiamo detto che l'acqua pura come quella distillata si comporta da isolante. L'acqua presente però sulla Terra è una soluzione contenente disciolta in essa sali, ioni ed altre sostanze che la rendono altamente conduttrice. Sali, basi o acidi sono dunque elettroliti che rendono l'acqua in cui essi sono disciolti una soluzione elettrolitica conduttrice.
La conducibilità elettrica di una soluzione è l'inverso della resistenza elettrica e rappresenta l'attitudine di un corpo a far fluire corrente elettrica quando si trova immerso in un campo elettrico. La sua unità di misura nel SI è il Siemens/metro [S/m] ed il simbolo per indicarla è σ:
σ = 1/R [S/m]
Un Siemens è l'inverso dell'Ohm : 1S = 1 Ω-1
Perché una soluzione elettrolitca conduce
La spiegazione del fatto che una soluzione elettrolitica conduce è da ricercare nella struttura microscopica elettrica degli atomi che compongono l'elettrolita. Prendiamo ad esempio il caso del cloruro di sodio il normale sale da cucina che troviamo disciolto nell'acqua e la rende altamente conducibile.
Questo sale è composto da un reticolo cristallino composto da ioni Sodio (Na+) e ioni cloruro (Cl−).
Il reticolo cristallino di questo sale è ben regolare e molto stabile in quanto le forze elettriche tra gli ioni sono intense. Tuttavia se del cloruro di sodio viene disciolto in acqua, le cui molecole sono polari cioè presentano una asimmetria tra la parte negativa e positiva delle molecole stesse, il reticolo cristallino si sfalda in quanto le molecole di acqua che hanno una costante dielettrica relativa εr pari a 80 si dispongono attorno agli ioni allineando le proprie parti negative e positive ed indeboliscono di 80 volte l'interazione elettrica tra gli ioni.
Il risultato è che il cristallo scompare e ioni positivi e negativi si separano muovendosi nella soluzione acquosa diventando portatori di carica in movimento che si allineano se immersi in un campo elettrico generando una corrente elettrica. Questo processo si chiama dissociazione elettrolitica.
Link correlati:
Che cos'è l'osmosi?
Che cosa sono le celle fotovoltaiche?
Come si calcola l'abbassamento crioscopico di una soluzione
Studia con noi