Tautomeria cheto-enolica
Tautomeria cheto-enolica e forma chetonica ed enolica
La tautomeria cheto-enolica è una particolare forma di isomeria di struttura caratteristica di molte aldeidi e di molti chetoni.
Quando una aldeide (o un chetone) ha adiacente al gruppo carbonilico un atomo di carbonio a cui è legato un idrogeno (idrogeno in alfa), può dare tautomeria cheto-enolica, ovvero un reazione di trasferimento protonico che trasforma una aldeide (o un chetone) in un enolo.
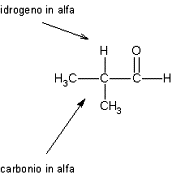
In questi casi la forma chetonica è in equilibrio con la forma enolica (enolica: da en, C=C ; olo, OH) e le due forme differiscono solo per la posizione di un idrogeno e del doppio legame:
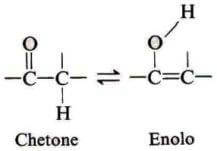
Un esempio è la tautomeria del 3-metil-2-butanone al 2-buten-2-olo:
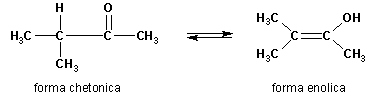
La forma chetonica e la forma enolica sono dette tautomeri e tranne che in completa assenza di acido o di base, sono in rapido equilibrio.
La forma chetonica e la forma enolica di un composto rappresentano due molecole distinte e differenti. La tautomeria pertanto non va confusa con la risonanza, le cui forme non hanno una reale esistenza fisica.
L'interconversione cheto-enolica è soggetta a catalisi sia acida che basica. Il processo può avvenire in più stadi o in modo sincrono.
Catalizzatore basico
Nella catalisi basica la base può estrarre il protone dal carbonio, generando lo ione enolato che può protonarsi all'ossigeno per dare l'enolo.
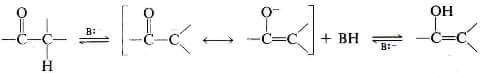
Catalizzatore acido
Nella catalisi acida si può avere protonazione sull'ossigeno del chetone portando all'acido coniugato del chetone, seguito dalla rimozione del protone del carbonio in α operata dalla base.
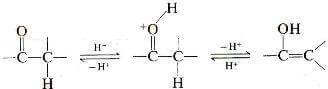
Alternativamente questi protoni possono trasferirsi in modo sincrono, e di solito si srive il processo proprio in questo modo:
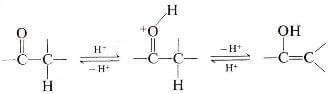
Eccetto che in completa assenza di acido di base le forme cheto-enoliche sono in rapida interconversione tra di loro, e quindi esistono in equilibrio mobile, la cui posizione dipende dai dettagli strutturali del composto e dalle condizioni sperimentali in cui si trova (solvente, temperatura, concentrazione, ecc.).
Studia con noi