Enantiomeri
Gli enantiomeri: immagini speculari non sovrapponibili
L'osservazione che esistevano numerose sostanze organiche di provenienza naturale otticamente attive, cioè capaci di far ruotare il piano della luce polarizzata indipendentemente dal loro stato fisico (quindi anche in soluzione allo stato liquido e di vapore), a differenza del quarzo in cui questa proprietà è limitata allo stato solido cristallino, è dovuta a J. B. Biot e risale al 1815.
Pasteur molto acutamente osservò che il fenomeno doveva essere attribuito a proprietà intrinseche delle molecole e giunse alla geniale intuizione che l'attività ottica delle suddette sostanze dovesse essere connessa con la particolare struttura asimmetrica delle molecole stesse (asimmetria molecolare) e che le modificazioni otticamente attive dovessero differire tra loro per la diversa disposizione nello spazio degli atomi.
Le proprietà geometriche del tetraedro sono tali che, se i quattro sostituenti dell'atomo di carbonio centrale sono differenti, la molecola non possiede piano di simmetria.
Esistono quindi due modi diversi (configurazioni) di sistemare la geometria della molecola; questi due modi differiscono per il fatto che non è possibile sovrapporre contemporaneamente tutti gli atomi di una figura a quelli dell'altra. Queste due configurazioni sono immagini speculari non sovrapponibili e vengono dette enantiomeri.
Una molecola che non è sovrapponibile alla sua immagine speculare è detta chirale.
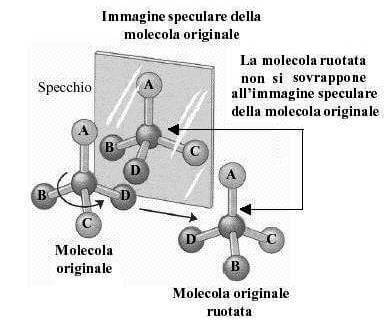
Immagini speculari non sovrapponibili
Due enantiomeri posseggono le stesse caratteristiche fisiche tranne per il fatto di ruotare il piano della luce polarizzata della stessa quantità ma in direzioni opposte.
L'enantiomero destrogiro (cioè quello che ruota il piano della luce polarizzata in senso orario) si indica con la lettere "d" o con "+", mentre l'enantiomorfo levogiro si indica con la lettera "l" o con il simbolo "-".
Mescolando in eguali quantità due enantiomeri si ottiene un miscuglio racemico che non fa ruotare il piano della luce polarizzata.
Se invece una molecola è sovrapponibile alla sua immagine speculare, non può dare luogo ad una coppia di enantiomeri ed esiste come un unico composto incapace di fare ruotare il piano della luce polarizzata.
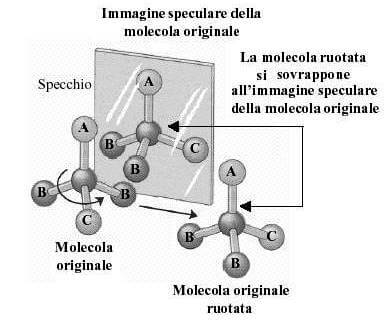
Immagini speculari sovrapponibili
Esercizi di stereochimica
Li trovi al seguente link: esercizi di stereochimica.
Studia con noi