Ka acido acetico
Quanto vale la Ka dell'acido acetico?
Vuoi sapere quanto vale la Ka dell'acido acetico?
Vuoi sapere il valore della Ka dell'acido acetico?
Se si, continua pure con la lettura dell'articolo.
L'acido acetico è un composto con formula chimica CH3COOH (talvolta scritta anche come CH3CO2H o C2H4O2), che presenta la seguente struttura:
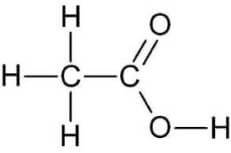
Valore della Ka dell'acido acetico
L'acido acetico perfettamente anidro non manifesta le sue proprietà acide; in presenza di acqua, invece, manifesta deboli proprietà acide.
In queste condizioni l'acido acetico ha una costante di dissociazione acida pari a:
Ka = 1,85 · 10-5 (a 25°C)
e si ionizza nel seguente modo:
CH3COOH ⇄ CH3COO− + H+
Si comporta quindi da acido monoprotico.
Pertanto, relativamente al valore della Ka dell'acido acetico, possiamo dire che, alla temperatura di 25°C, vale:
![]()
Esercizio
Quali sono la [H+] e il pH di una soluzione 0,1M di acido acetico CH3COOH?
Ka (CH3COOH) = 1,8 · 10-5
Lo svolgimento dell'esercizio lo trovi qui: pH di una soluzione di acido acetico.
Esercizio di elevata difficoltà
1L di una soluzione acido acetico avente pH=3 di viene aggiunta a 1L di una soluzione di acido acetico avente pH=4.
Calcolare il pH della soluzione risultante sapendo che Ka (CH3COOH) = 1,8 · 10-5
Lo svolgimento dell'esercizio lo trovi qui: pH della soluzione ottenuta unendo due soluzioni di acido acetico a diversa concentrazione.
Link correlati:
Quando una base è forte? Quando un acido è forte?
Che cosa afferma la teoria di Arrhenius?
Tabella con i valori della Ka e della Kb dei principali acidi e basi
Studia con noi