Differenza tra orbita e orbitale
Qual è la differenza tra orbita e orbitale?
I termini orbita e orbitale si riferiscono al moto degli elettroni attorno al nucleo in modelli atomici differenti.
Più in particolare, il termine orbita si riferisce alla traiettoria assunta dagli elettroni quando si muovono attorno al nucleo secondo orbite circolari di ben definita energia (orbite stazionarie o livelli di energia).
Infatti, in questa tipologia di moto degli elettroni attorno al nucleo, prevista dal modello atomico di Bohr, l'elettrone ruota a velocità v, su orbite circolari di raggio R.
Il modello citato ricorda in scala il Sistema Solare: attorno al Sole (che rappresenta il nucleo dell'atomo) si muovono i pianeti (che rappresentano gli elettroni) su orbite circolari di raggio R.
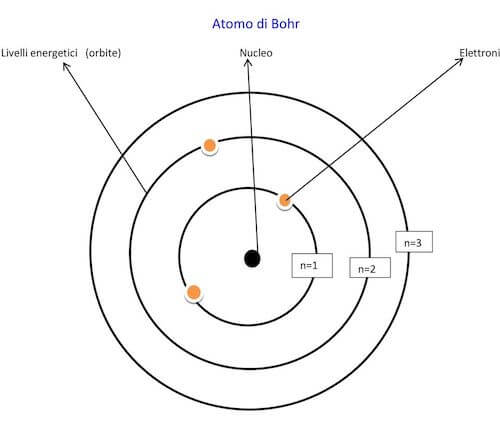
Secondo il modello atomico di Bohr gli elettroni si muovono attorno al nucleo su orbite circolari allo stesso modo in cui pianeti si muovono attorno al Sole.
Il modello atomico di Bohr, seppur molto esaustivo nello spiegare alcuni fenomeni fisici legati all'atomo, risultava lacunoso per altri.
Si ritenne necessario introdurre modelli atomici più esaustivi, cosa che avvenne con il fisico tedesco E. Schrodinger (premio Nobel nel 1933).
Secondo il modello atomico di Schrodinger, noto anche come modello atomico a orbitali, gli elettroni si muovono attorno al nucleo in zone specifiche dette appunto "orbitali".
Racchiudendo entro una superficie limitante tutti i punti per i quali l'elettrone ha la massima probabilità di passare nel suo moto intorno al nucleo, si ottiene una figura geometrica, simmetrica rispetto al nucleo stessa, che dà un idea della "forma" dell'orbitale.
Gli orbitali possono avere forme diverse; il più semplice di essi è l'orbitale di tipo s, in cui l'elettrone si muove all'interno di una sfera al cui centro è presente il nucleo dell'atomo.
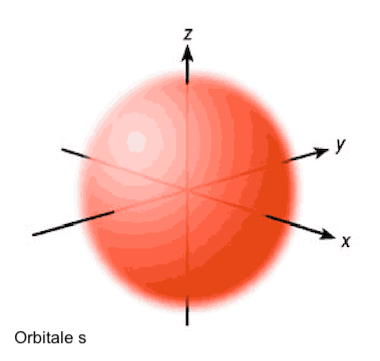
L'orbitale è una zona attorno al nucleo in cui è massima la probabilità di trovare l'elettrone. In un orbitale di tipo s (come quello rappresentato in figura) la probabilità di trovare l'elettrone è massima all'interno della sfera.
Quindi, mentre il modello atomico di Bohr suppone che gli elettroni si muovono intorno al nucleo secondo orbite circolari, il modello atomico di Schrodinger definisce le regioni dello spazio attorno al nucleo in cui è massima la probabilità di trovare gli elettroni: tali regioni sono dette orbitali.
Link correlati:
Che cos'è la meccanica razionale?
Che cosa sono le orbite ellittiche?
Che cosa sono le regole di selezione?
Studia con noi