Carbeni
Struttura elettronica e reattività dei carbeni
Il carbene è una specie chimica con formula R2C: in cui l'atomo di carbonio ha due elettroni non impegnati in legami.
Estremamente reattivi, i carbeni esistono come intermedi di particolari di particolari reazioni chimiche in cui si comportano da forti elettrofili.
Il più semplice carbene è il metilene :CH2 che, derivato dal diiodometano, attacca il doppio legame di alcheni generando ciclopropani (reazione di Simmons-Smith).
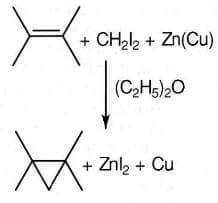
Di seguito altre reazioni di carbeni che si addizionano ai doppi legami degli alcheni.
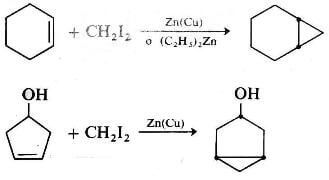
L'addizione di atomi di carbonio bivalente agli alcheni è il metodo più semplice con cui ottenere ciclopropani.
Strutture elettroniche dei carbeni
Esistono due tipi di strutture che possono essere fatte corrispondere al carbene.
I due elettroni del guscio di valenza che non vengono utilizzati nei legami possono essere entrambi nello stesso orbitale (nel qual caso l'altro rimane vuoto) e la molecola nel suo complesso può essere vista come un carbanione (orbitale con due elettroni) e carbocatione (orbitale vuoto) contemporaneamente.
Alternativamente i due elettroni possono trovarsi in due differenti orbitali e la molecola può essere vista come un diradicale. In quest'ultimo caso la molecola può avere gli elettroni appaiati (singoletto) o spaiati (tripletto). Come è possibile notare nella figura seguente, quest'ultimo caso è il più stabile.
Il singoletto in cui i due elettroni, pur avendo spin accoppiato, si trovano uno in ciascun orbitale a disposizione, può essere considerato come uno stato eccitato del singoletto, in cui entrambi gli elettroni sono nello stesso orbitale. Tale stato eccitato deve avere un'esistenza molto breve e deve rapidamente ricadere allo stato fondamentale.
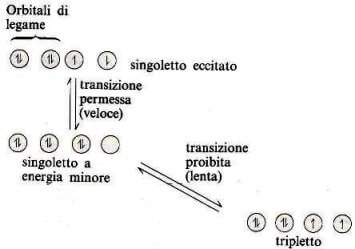
Correlazione fra diverse possibili strutture elettroniche di un carbene tipico.
Il carbene tripletto e quello singoletto, con due elettroni appaiati nello stesso orbitale, dovrebbero avere un'energia comparabile. Praticamente può esistere l'una o l'altra struttura a seconda delle circostanze. Normalmente lo stato di tripletto è lo stato fondamentale e lo stato di singoletto è lo stato eccitato.
Le transizioni tra lo stato di tripletto e quello di singoletto sono proibite e avvengono lentamente, per cui è possibile preparare un cabene in condizioni di singoletto e farlo reagire prima che diventi tripletto. Alternativamente si può fare divenire il singoletto tripletto e poi sottoporlo a reazione.
Studia con noi