Legge di Dalton
Enunciato e spiegazione della legge di Dalton delle pressioni parziali dei gas
La legge di Dalton afferma che: quando due o più gas vengono mescolati in unico recipiente, senza che tra essi avvenga alcuna reazione chimica, la pressione totale esercitata dalla miscela gassosa è uguale alla somma delle pressioni parziali esercitate dai singoli componenti. In altri termini:
![]()
In questa equazione, il componente imo, si comporta dunque come se fosse da solo e contribuisce alla pressione totale in proporzione al numero di moli.
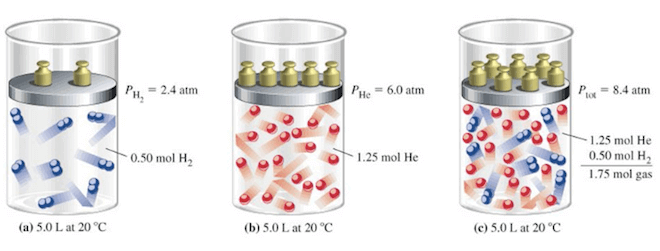
Mantenendo la temperatura costante, la pressione totale nel recipiente di destra contenente sia H2 che He è la somma delle pressioni esercitate dai singoli gas.
Inoltre, la pressione parziale di ciascun gas che fa parte di una miscela di gas a comportamento ideale, è uguale alla pressione che quel gas eserciterebbe se occupasse da solo il volume occupato dalla miscela.
Per ciascuno degli n gas presenti in una miscela gassosa è applicabile l'equazione di stato e, indicando con ni e Pi il numero di moli e la pressione parziale del componente imo e con V il volume occupato dalla miscela gassosa, si può perciò scrivere:
![]()
Dividendo membro a membro l'equazione precedente per l'equazione:
![]()
si ottiene:
![]()
che indica un modo per determinare la pressione parziale del componente imo, dove il rapporto
![]()
esprime la frazione molare del componente imo. Pertanto potremmo scrivere:
![]()
e quindi la pressione parziale di ciascuno dei componenti di una miscela gassosa è data dal prodotto della pressione totale per la frazione molare di quel componente.
In altre parole: la pressione parziale del componente imo di una miscela gassosa di pressione totale Ptot è data dal prodotto della frazione molare del componente imo per il valore della pressione totale Ptot.
Spiegazione e conseguenze della legge di Dalton
L'equazione di stato del gas ideale è valida quale che sia la natura chimica delle particelle gassose; ad una data temperatura e per un dato volume, la pressione di un gas è quindi determinata soltanto dal numero delle particelle.
Pertanto se in un volume V sono contenute ad esempio 10 moli gassose che alla temperatura T esercitano una pressione P, ciascuna di queste moli esercita mediamente una pressione pari ad ⅒ di P, indipendentemente dal fatto che le 10 moli siano della stessa specie chimica o di specie chimiche diverse.
Ciò significa che se, ad esempio, delle 10 moli 4 sono moli N2 e 6 sono moli H2, il 40% della pressione totale (Ptot) è dovuta all'azoto (pressione parziale dell'N2: PN2) ed il 60% all'idrogeno (pressione parziale dell'H2: PH2).
Si supponga ora di disporre di due recipienti rigidi di volume uguale (V), ciascuno munito di manometro, immersi in un termostato a temperatura T e contenenti due gas diversi A ,B alla stessa pressione (P).
Se i due recipienti vengono messi in comunicazione fra loro, si osserva che il valore della pressione (P) si mantiene costante in ciascuno dei due recipienti durante la diffusione del gas A nel recipiente che contiene il gas B (e viceversa).
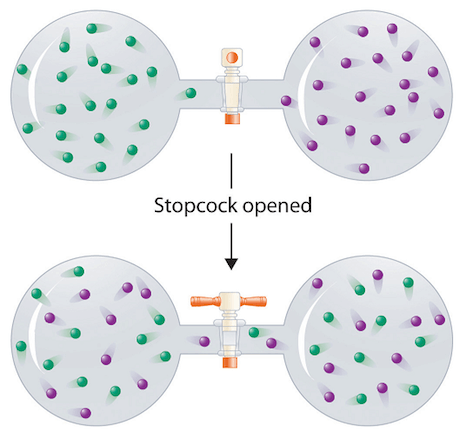
Due recipienti rigidi mantenuti a temperatura costante e contenenti due gas diversi, vengono messi in comunicazione fra loro: si osserva la diffusione del gas A nel recipiente che contiene il gas B (e viceversa).
Dopo un certo tempo la diffusione sarà completata e ciascuno dei due gas occuperà un volume doppio (2V) del volume iniziale e la pressione di ciascuno di essi sarà perciò (legge di Boyle) dimezzata rispetto a quella iniziale. Possiamo quindi scrivere:
PA = P/2
PB = P/2
PA + PB = Ptot
Esercizio sulla legge di Dalton
Una miscela gassosa è costituita da 8,802 g di CO2, 5,60 g di N2 e 1,60 g di He. Sapendo che, ad una certa temperatura, la pressione totale esercitata dalla miscela gassosa è di 4 atm, si determini la pressione parziale di ciascun componente.
Svolgimento dell'esercizio
Calcoliamo inizialmente le masse molari dei composti:
MM (CO2) = 44,01 g/mol
MM (N2) = 28,00 g/mol
MM (He) = 4,00 g/mol
Determiniamo il numero di moli di ciascun componente dividendo la massa in grammi per il valore della massa molare:
nCO2 = g / MM = 8,802 / 44,01 = 0,20 mol
nN2 = g / MM = 5,60 / 28,00 = 0,20 mol
nHe = g / MM = 1,60 / 4,00 = 0,40 mol
Le moli totali della miscela gassosa sono:
ntot = 0,20 + 0,20 + 0,40 = 0,80 mol
Calcoliamo infine le frazioni molari di tutti i componenti dividendo il numero di moli di ciascun componente per il numero di moli totali:
a) Frazione molare di CO2:
XCO2 = 0,20 / 0,80 = 0,25
a) Frazione molare di N2:
XN2 = 0,20 / 0,80 = 0,25
a) Frazione molare di He:
XHe = 0,40 / 0,80 = 0,50
In base alla legge di Dalton la pressione parziale di ciascun componente della miscela gassosa è data dal prodotto della pressione totale (Ptot = 4 atm) per la frazione molare di quel componente (Xi). In formule:
PCO2 = Ptot · XCO2 = 4 · 0,25 = 1,0 atm
PN2 = Ptot · XN2 = 4 · 0,25 = 1,0 atm
PHe = Ptot · XHe = 4 · 0,50 = 2,0 atm
Esercizi sui gas
Li trovi online e svolti al seguente link: esercizi sui gas.
Link correlati:
Esercizio sul calcolo della pressione di una miscela di gas
Esercizio sul calcolo della pressione totale di due gas
Studia con noi