Fattori che influenzano la velocità di reazione
Quali sono i fattori che influenzano la velocità di una reazione chimica
La velocità delle reazioni chimiche dipendono dai seguenti fattori:
- natura e concentrazione dei reagenti;
- area della superficie di separazione (superficie di contatto);
- temperatura;
- presenza di catalizzatori.
Natura dei reagenti
La velocità di una reazione chimica dipende dalla natura dei reagenti. Per esempio, il sodio reagisce vigorosamente con l'acqua mentre un altro metallo dello stesso gruppo, il potassio, reagisce in un modo quasi esplosivo.
La reazione è la stessa ma la velocità di reazione è diversa poiché sono diverse le caratteristiche e la natura dei reagenti.
Concentrazione dei reagenti
L'influenza della concentrazione dei reagenti sulla velocità di reazione, può essere facilmente compresa se si tiene conto che per reagire, due particelle devono venire in reciproco contatto.
È chiaro che, maggiore è la concentrazione dei reagenti, più è probabile un loro reciproco contatto.
Questo ragionamento però è valido solo se la reazione avviene in un unica fase (gassosa o liquida).
Se la reazione avviene in fase eterogenea (per esempio solida-liquida), anziché la concentrazione dei reagenti bisogna considerare l'area della superficie di separazione ovvero la superficie di contatto tra le due fasi.
Superficie di contatto
Se la reazione avviene in fase eterogenea, cioè se i reagenti sono presenti in più fasi (esempio solida-liquida), la velocità delle reazioni chimiche dipende dalla superficie di contatto tra le due fasi.
Tanto maggiore è la superficie di contatto tanto maggiore è la velocità di reazione.
Per esempio un pezzo di carbone brucia lentamente all'aria ma se viene ridotto in forma di polvere finissima, la combustione procede in modo talmente veloce che la reazione può essere anche esplosiva.
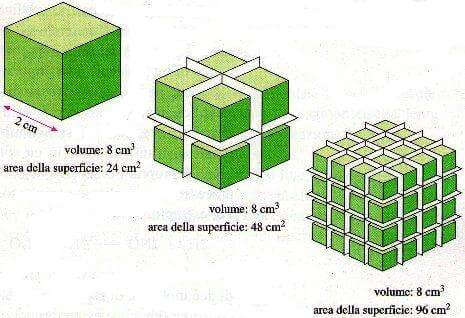
Nei tre casi, pur essendo uguale il volume, la sempre maggiore suddivisione del reagente allo stato solido determina un aumento della superficie di contatto con il liquido in cui è immerso e quindi un aumento della velocità di reazione.
Temperatura
Come regola del tutto generale e quindi puramente orientativa, un aumento di temperatura di 10°C può fare raddoppiare ma anche triplicare la velocità di una reazione chimica.
Un applicazione di questo principio si ha nella conservare degli alimenti nella quale si ricorre alla refrigerazione che, mediante un abbassamento di temperatura, determina una diminuzione della velocità di decomposizione dei cibi.
Catalizzatori
Un'idea dell'influenza dei catalizzatori sulla velocità delle reazioni chimiche, può essere data considerando una miscela di idrogeno ed ossigeno che a temperatura ambiente può rimanere inalterata anche per tempi lunghissimi ma che, in presenza di un opportuno catalizzatore (es. platino spugnoso), reagisce in modo esplosivo con produzione di acqua. Per approfondimenti: influenza dei catalizzatori sulla velocità delle reazioni chimiche.
Studia con noi