Esercizi calorimetria
Esercizi online e gratuiti sulla calorimetria
Vengono di seguito proposti alcuni esercizi di calorimetria.
La raccolta degli esercizi di calorimetria di seguito proposta è rivolta sia agli studenti universitari delle facoltà scientifiche che agli studenti di licei ed istituti tecnici.
Prima di affrontare gli esercizi di calorimetria facciamo una breve introduzione ai fenomeni relativi agli scambi di calore tra corpi.
Il calore è una forma di energia che viene scambiata tra corpi che si trovano a temperature differenti.
Il simbolo per indicare la quantità di calore scambiata è Q la cui unità di misura è il joule, simbolo [J].
Un'unità di misura utilizzata per il calore è anche la Kcal e vale che
1 Kcal = 4186 J
Il calore acquisito o ceduto da un corpo è dato da:
Q = m · c · ΔT
in cui
m è la massa del corpo e si misura in kg
c è il calore specifico che si misura in J/(kg ·°C)
ΔT è la differenza di temperatura.
Per l'acqua il calore specifico vale:
cacqua = 4186 J/(kg ·°C)
Quando un corpo più caldo viene posto a contatto con un corpo più freddo, i due corpi tendono a portarsi alla stessa temperatura detta temperatura di equilibrio Te, per cui sarà:
Qacquisito = - Qceduto
Durante un passaggio di stato la temperatura rimane costante ed il calore necessario a completare il processo è dato:
Qf = m ·λf
oppure
Qv = m · λv
in cui Qf e Qv sono rispettivamente il calore da fornire/sottrarre per dar corso alla fusione (solidificazione) o alla vaporizzazione (condensazione) e λf e λv sono invece detti calori latenti di fusione e vaporizzazione e si misurano in J/kg.
Chimica-online.it inoltre ti offre anche una calcolatrice scientifica.
Esercizi calorimetria
Di seguito gli esercizi di calorimetria elencati secondo un ordine crescente di difficoltà.
Livello di difficoltà medio-basso
1.
Quanto calore occorre per riscaldare 1,5 l di acqua che si trova a temperatura ambiente ( 20°C) fino a portarla alla temperatura finale di 80 °C?
Lo svolgimento dell'esercizio lo trovi qui: esercizio sulla legge fondamentale della termologia.
2.
Quanto calore bisogna fornire per fondere completamente un cubetto di ghiaccio il cui lato misura 1 dm?
Si sappia che il calore latente di fusione dell'acqua è pari a 335,2 KJ/kg.
Lo svolgimento dell'esercizio lo trovi qui: calcolo del calore necessario per fondere un cubetto di ghiaccio.
3.
Una massa di 1,5 kg di alluminio viene riscaldata dalla temperatura di 20°C alla temperatura di 90°C.
Si determini la quantità di calore, espressa in kcal, da fornire al blocco di alluminio.
Si sappia che il calore specifico dell'alluminio è di 0,22 cal/(g·°C).
Lo svolgimento dell'esercizio lo trovi qui: massa di 1,5 kg di alluminio viene riscaldata da 20°C a 90°C. Calcolo delle kcal.
4.
Le pareti di un edificio sono costituite in cemento (λ = 1.1 W/(m∙°C) ); il loro spessore è di 20 cm mentre la superficie totale è di 300 m2.
Sapendo che la differenza di temperatura fra la superficie interna ed esterna è di 15 °C, qual è la quantità di calore scambiata in un giorno?
Lo svolgimento dell'esercizio lo trovi qui: calcolo del calore scambiato tra due pareti a differente temperatura.
5.
Determinare lo spessore di una parete costituita da mattoni refrattari (λ = 1 kcal/(h m °C)) sapendo che essa è larga 4 m ed alta 6 m e che la superficie interna si trova a 28°C mentre quella esterna è a 4°C, se si vuole che il flusso termico areico non superi i 100 W/m2.
Lo svolgimento dell'esercizio lo trovi qui: calcolo dello spessore di una parete.
6.
Calcolare la potenza termica scambiata tra una finestra di vetro e l'esterno sapendo che la temperatura intera è di 20°C mentre la temperatura esterna è -5°C e la superficie della finestra è di 0,60 m2.
Si sappia che la conducibilità termica del vetro è pari a λe = 23,26 W/(m∙K).
Lo svolgimento dell'esercizio lo trovi qui: calcolo della potenza termica.
7.
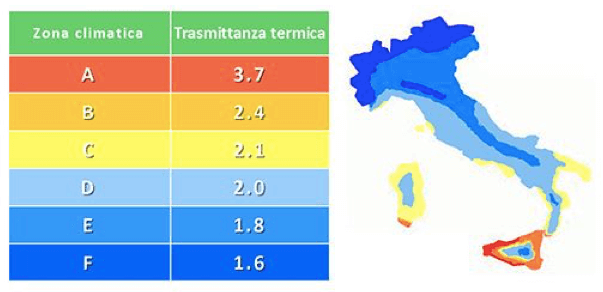
Si vuole realizzare un tetto in mattoni in zona termica E. Si ha a disposizione la seguente tabella con l'evidenza delle diverse zone termiche in Italia.
Sapendo che la conducibilità termica dei mattoni è λ = 0,90 W/(m·K), si determini lo spessore del tetto da realizzare.
Lo svolgimento dell'esercizio lo trovi qui: esercizio sulla trasmittanza termica.
8.
Si hanno a disposizione 30 cm di mattoni e 5 cm di polistirolo XPS per costruire una parete isolante termica.
1) Quale delle due soluzioni è la migliore?
2) Se invece si mettono in serie i mattoni con 10 cm di polistirolo dello stesso tipo quale resistenza termica si ottiene?
Si sappia che per i mattoni λ = 0,90 W/(m·K) e per il polistirolo λ = 0,040 W/(m·K).
Lo svolgimento dell'esercizio lo trovi qui: esercizio sulla resistenza termica.
Livello di difficoltà medio-alto
9.
Quanto calore è necessario per fondere un blocco di ghiaccio di 10 kg che si trova ad una temperatura di -10°C ed avere acqua liquida alla temperatura di 60°?
Si sappia che:
calore specifico del ghiaccio = 2260 J/kg;
calore latente di fusione dell'acqua = 335,2 KJ/kg
Lo svolgimento dell'esercizio lo trovi qui: calore necessario per fondere il ghiaccio.
10.
Un blocco di ferro di massa 500 g ed alla temperatura iniziale di 145,0 °C viene immerso in 250 g di acqua alla temperatura di 20,0 °C.
Sapendo che non ci sono dispersioni termiche, calcolare la temperatura di equilibrio che raggiunge il sistema.
Calore specifico del ferro = 452 J/(kg ·°C)
Lo svolgimento dell'esercizio lo trovi qui: calcolo della temperatura di equilibrio.
11.
Un blocco di 12 kg di alluminio alla temperatura di 420 K è immerso in una vasca che contiene 30 L di acqua alla temperatura di 303 K.
Determina la temperatura di equilibrio raggiunta dall'alluminio e dall'acqua. Trascura ogni forma di dispersione termica.
Si sappia che il calore specifico dell'alluminio è pari a 880 [J/kg°K] mentre il calore specifico dell'acqua è pari a 4186 [J/kg°K].
Lo svolgimento dell'esercizio lo trovi qui: temperatura di equilibrio raggiunta dall'alluminio e dall'acqua.
12.
Un recipiente costituito di un metallo sconosciuto ha una massa di 4 kg e contiene al suo interno 15 litri di acqua.
Inizialmente il sistema si trova alla temperatura di 15,5 °C.
Ad un certo punto si immerge nell'acqua un corpo costituito dallo stesso metallo del recipiente e di massa 2 kg alla temperatura di 182°C.
Sapendo che la temperatura finale del sistema è di 18,3 °C, determinare il calore specifico del metallo costituente sia il recipiente sia il pezzo introdotto nell'acqua.
Lo svolgimento dell'esercizio lo trovi qui: calcolo del calore specifico di un metallo incognito.
13.
Un blocco di ghiaccio di massa 500 g ed alla temperatura di 0°C viene immerso in una pentola contenente 500 g di acqua bollente a 100 °C.
Determinare lo stato finale del sistema e la temperatura raggiunta.
Calore latente di fusione dell'acqua = 335,2 KJ/kg
Lo svolgimento dell'esercizio lo trovi qui: esercizio sull'equilibrio termico.
Studia con noi