Nitrosazione delle alchilammine
Formazione di N-nitrosammine e reazione di deamminazione
Quando una soluzione di nitrito di sodio (NaNO2) viene acidificata con acido cloridrico diluito o con acido solforico diluito, vengono generate numerose specie chimiche che possono agire come sorgenti del catione nitrosile, tra le quali la più importante è l'acido nitroso.
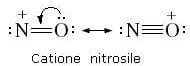
L'acido nitroso viene solitamente preparato in situ poiché è altamente instabile e reagisce anche con l'umidità presente nell'atmosfera.
La sequenza di reazioni che portano alla formazione del catione nitrosile può essere riassunta come qui di seguito:
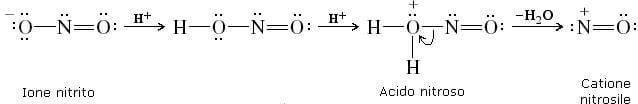
Reazioni delle ammine secondarie con l'acido nitroso
Le ammine secondarie reagiscono con l'acido nitroso portando alla formazione di N-nitrosammine.
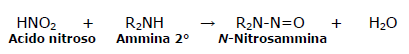
La formazione della N-nitrosammina avviene per attacco nucleofilo dell'ammina all'atomo di azoto dello ione nitrosile.
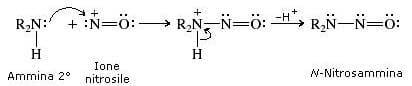
Reazioni delle ammine terziarie con l'acido nitroso
Le ammine terziarie reagiscono in modo complesso con l'acido nitroso. La reazione è di importanza limitata.
Reazioni delle ammine primarie con l'acido nitroso
Le ammine primarie alifatiche reagiscono con l'acido nitroso per dare i sali di diazonio che sono troppo reattivi per essere isolati (a differenza di quanto avviene per i corrispondenti sali derivanti dalle ammine aromatiche primarie).
![]()
Una volta formati, i sali di diazonio perdono facilmente una molecola di azoto molecolare generando un carbocatione.
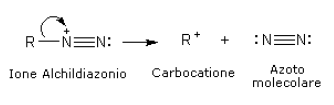
Pertanto, la reazione di una ammina primaria con acido nitroso porta alla perdita del gruppo amminico e alla formazione di un carbocatione. Per tale motivo tale reazione è anche detta deamminazione.
Il carbocatione generato può andare incontro ad una varietà di reazioni, portando a delle miscele che possono contenere alcoli, olefine, ciclopropani e anche alogenuri se è presente lo ione alogeno. Spesso nei prodotti finali lo scheletro degli atomi di carbonio è riarrangiato.
Tali reazioni, anche se poco utili ai fini pratici, sono importanti perché permettono di studiare il comportamento dei carbocationi generati dalla reazione.
Studia con noi