Saggio per il riconoscimento dello ione ammonio
Reazione chimica con sviluppo di ammoniaca NH3
Attrezzature
Becco Bunsen
Treppiede
Reticella spargifiamma
Bagnomaria per provette
Provette
Tubicino di vetro piegato a squadra o a U con tappo forato
Materiali e reagenti
Cloruro di ammonio NH4Cl
Soluzione di idrossido di sodio NaOH
Fenolftaleina
Cartina all'indicatore universale
Acqua distillata
Procedimento
In una provetta porre qualche mL di acqua distillata e 2-3 gocce di indicatore fenolftaleina.
In una seconda provetta porre una piccola quantità di cloruro di ammonio NH4Cl e qualche mL della soluzione di idrossido di sodio NaOH.
Dalla seconda provetta si ha sviluppo di ammoniaca NH3 secondo la reazione:
NH4Cl + NaOH → NaCl + H2O + NH3
La presenza di ammoniaca è riconoscibile dal caratteristico odore.
Avvicinare all'imboccatura della seconda provetta un pezzetto di cartina all'indicatore universale inumidita con acqua. Si osserva il viraggio del colore della cartina al verde-blu.
Mediante un tubo a squadra munito di tappo fare gorgogliare il gas nella soluzione della prima provetta.
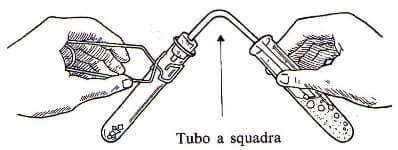
Per facilitare la reazione e far dilatare il gas sviluppato, riscaldare a bagnomaria la provetta contenente i reattivi. Il colore dell'indicatore fenolftaleina presente nella prima provetta vira al rosso-violaceo in seguito alla formazione degli ioni ossidrile.
NH3 + H2O → NH4+ + OH−
Questa reazione può essere utilizzata come saggio per il riconoscimento della presenza dello ione ammonio (NH4+) in una sostanza.
Studia con noi