Solvente
Componenti di una soluzione: il solvente
I solventi sono tutto ciò che permette di portare una sostanza (detta soluto) in soluzione; solvente è dunque in senso lato anche un gas in cui se ne trova disperso un altro o un solido che discioglie un altro solido (soluzione solida). Le soluzioni sono infatti dispersioni omogenee di due (o più) specie chimiche una nell'altra, in proporzioni variabili; il solvente è il componente della soluzione presente in maggior quantità.
Comunemente si dà tuttavia il nome di solvente a un liquido che discioglie una o più sostanze, solide, liquide o gassose che siano.
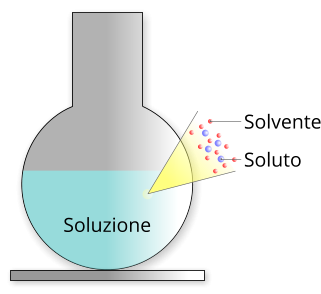
Componenti di una soluzione liquida: il solvente scioglie il soluto.
La soluzione più semplice è costituita da un'unica specie chimica come solvente e da un'unica specie chimica come soluto (ad esempio zucchero sciolto in acqua), ma possono esistere soluzioni in cui si hanno più soluti.
È d'uso comune indicare col nome di solvente il componente della soluzione che si presenta nello stesso stato di aggregazione di quest'ultima ed è solitamente quello presente in maggior quantità.
Così, ad esempio, unendo zucchero (solido) ed acqua (liquida), la soluzione che si ottiene è liquida: si dice pertanto che l'acqua è il solvente e lo zucchero è il soluto.

Se solvente e soluto hanno lo stesso stato di aggregazione, (ad esempio acqua ed etanolo, ambedue liquidi) si indica come solvente la specie presente in quantità molecolarmente maggiore.
Talvolta non è possibile in base a queste regole fare differenze tra solvente e soluto: se si considera, ad esempio, una soluzione costituita da un ugual numero di molecole di acqua ed etanolo, ambedue liquidi, può parlarsi indifferentemente di soluzione acquosa di alcol o di soluzione alcolica di acqua (anche se usualmente si preferisce la prima dizione).
Il solvente in una soluzione può essere in tutti gli stati di aggregazione: solido (come il ferro nell'acciaio), liquido (come l'acqua nell'acqua minerale) e gassoso (come l'azoto nell'aria).
Esistono infatti diversi tipi di soluzione:
Soluzioni gassose costituite da un solvente gassoso che discioglie un soluto gassoso (ossigeno miscelato ad azoto).
Soluzioni liquide, possono essere costituite da:
- solvente liquido che discioglie soluto gassoso (acqua che discioglie O2);
- solvente liquido che discioglie soluto liquido (H2O che discioglie etanolo);
- solvente liquido che discioglie soluto solido (acqua che discioglie sale).
Soluzioni solide, possono essere costituite da:
- solvente solido che discioglie soluto gassoso (palladio che discioglie H2);
- solvente solido che discioglie soluto liquido (cadmio che discioglie Hg);
- solvente solido che discioglie soluto solido (argento che discioglie rame).
Solvente universale
Con il termine "solvente universale" viene indicata l'acqua, non perché essa sciolga tutte le sostanze, ma perché ne scioglie un notevole numero tra le più comuni - elettroliti e non elettroliti - ed è il liquido di gran lunga più diffuso. Esso ha, anche come solvente, caratteristiche del tutto peculiari.
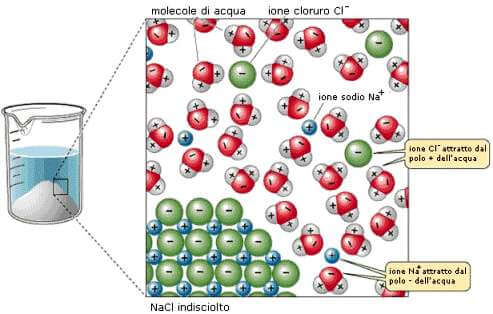
Processo di dissoluzione del cloruro di sodio NaCl (soluto) da parte dell'acqua (solvente).
Ricordiamo però che solventi possono essere sia composti organici più o meno semplici, ma anche prodotti inorganici come l'ammoniaca liquida, l'acido fluoridrico liquido e lo stesso acido solforico, dalle capacità solventi elevate.
I solventi appartengono a classi assai disparate di sostanze organiche e comprendono quindi idrocarburi, composti clorurati, alcoli, chetoni, esteri, eteri e, per qualche applicazione, nitroparaffine, ammine e altri prodotti organici. Le caratteristiche delle singole classi, legate a numerose proprietà ma in modo particolare alla polarità dei vari tipi molecolari, guidano nella scelta per le singole applicazioni, ovviamente in relazione alle caratteristiche del soluto o dei soluti.
Tuttavia, in senso più ristretto, il termine solvente si riserva a quelle sostanze che si impiegano per trasferirne un'altra, o più, da un punto a un altro. Il concetto può essere chiarito dalla esemplificazione: l'estrazione di un composto solubile da un solido, come quella dell'olio dai semi oleosi, si opera con un solvente; analogamente l'estrazione selettiva di un costituente da una miscela liquida, come si opera nell'industria petrolifera o nell'estrazione di taluni antibiotici dai liquidi di coltura, si realizza ricorrendo a un solvente selettivo.
Studia con noi