Elettrodo standard a idrogeno
L'elettrodo standard ad idrogeno come elettrodo di riferimento
La semicella assunta come riferimento nel calcolo dei potenziali di riduzione standard di ogni elettrodo, è nota come elettrodo standard ad idrogeno ed è costituita dalla coppia redox H+/H2.
Tale semicella è costituita da una lamina di platino immersa in una soluzione 1M di ioni H+, nella quale viene fatto gorgogliare idrogeno alla pressione parziale di 1 atm.
La reazione di riduzione che avviene è la seguente:
![]()
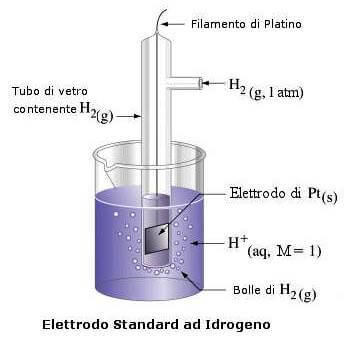
A tale semicella viene attribuito, in modo convenzionale, il potenziale zero.
Si attribuisce invece un potenziale positivo a qualsiasi coppia redox la cui semicella, collegata ad una semicella ad idrogeno, subisce riduzione.
Viceversa, si attribuisce un potenziale negativo a qualsiasi coppia redox la cui semicella, collegata ad una semicella ad idrogeno, subisce ossidazione.
L'elettrodo standard ad idrogeno può funzionare quindi, a seconda della casi sia da anodo che da catodo.
I potenziali in tal modo misurati prendono il nome di potenziali standard di riduzione.
Determinazione del potenziale standard di riduzione della coppia Zn2+/Zn
Supponiamo di collegare un elettrodo standard ad idrogeno con un elettrodo formato da una lamina di zinco immersa in una soluzione 1M dei suoi ioni (coppia redox Zn2+/Zn).
In queste condizioni il voltmetro segna una differenza di potenziale di 0,76 V.
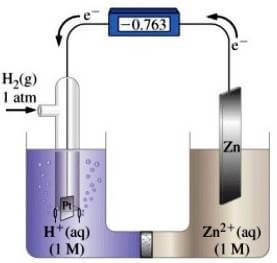
Zn/Zn2+ // H+/H2
Il pH della soluzione catodica (rappresentata a sinistra) aumenta gradualmente: ciò significa che lo zinco si ossida a Zn2+ cedendo elettroni agli ioni H+ che si riducono a H2.
Zn → Zn2+ + 2e−
2H+ + 2e− → H2
------------------------
Zn +
2H+ → Zn2+ + H2
Pertanto:
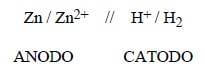
La coppia Zn2+/Zn ha pertanto una minor tenenza a ridursi rispetto alla coppia H+/H2 e quindi alla coppia Zn2+/Zn viene assegnato un potenziale standard di riduzione negativo pari a E° = - 0,76V.
Link correlati:
Come è fatto un elettrodo a calomelano?
Calcolo del potenziale di un elettrodo a idrogeno in condizioni non standard
Studia con noi