Indicatori di pH
Caratteristiche e funzionamento degli indicatori di pH
Gli indicatori di pH sono acidi o basi organici deboli a elevato peso molecolare, che assumono colorazioni diverse a seconda del pH.
Se indichiamo con HIn l'indicatore indissociato, esso in soluzione acquosa si dissocia secondo la reazione:
![]()
dove In− rappresenta la base coniugata di HIn.
pH di viraggio di un indicatore
Per un dato indicatore, si definisce pH di viraggio il pH in corrispondenza del quale la concentrazione molare dell'acido indissociato HIn è uguale alla concentrazione molare (= molarità) della sua base coniugata In−, cioè il pH al quale si realizza la seguente condizione:
![]()
Il pH di viraggio di un indicatore si può calcolare quando è nota la sua costante di dissociazione KHIn :
![]()
Poiché, come si è visto, per definizione di pH di viraggio [HIn] = [In−], semplificando i due termini nella formula precedente, si ha:
![]()
da cui, per definizione di pH, si ha:
![]()
Il pH di viraggio ha dunque un valore numerico bel definito.
Intervallo di viraggio di un indicatore
L'intervallo di viraggio indica il campo di variazione di pH che si deve produrre perché l'occhio umano possa percepire la variazione di colore dalla forma acida a quella basica e viceversa.
Normalmente, l'intervallo di viraggio si estende per circa due unità di pH, all'inteno dei quali il pH di viraggio occupa la posizione centrale.
Come si sa, ogni unità di pH differisce da quella immediatamente successiva o da quella immeditamente precedente per una differenza di [H+] di 10 volte.
Quindi perché l'occhio dell'osservatore possa distinguere nettamente il passaggio da un colore all'altro è necessario che nella soluzione sia presente un eccesso di una delle due forme (HIn / In−) rispetto all'altra di almeno 10 volte.
Ne segue che il colore tipico della forma acida dell'indicatore HIn è nettamente distinguibile quando:
![]()
Introducendo questo valore nella formula già vista:
![]()
si ha:
![]()
da cui, applicando semplici calcoli matematici e le proprietà dei logaritmi, si ha:
![]()
Analogamente, il colore tipico della forma basica dell'indicatore (In−) è nettamente distinguibile quando:
![]()
L'intervallo di viraggio dell'indicatore di pH sarà dunque pari a:
![]()
In una titolazione acido/base si sceglie l'indicatore il cui viraggio è il più possibile vicino al punto di equivalenza.
Tipi di indicatori di pH
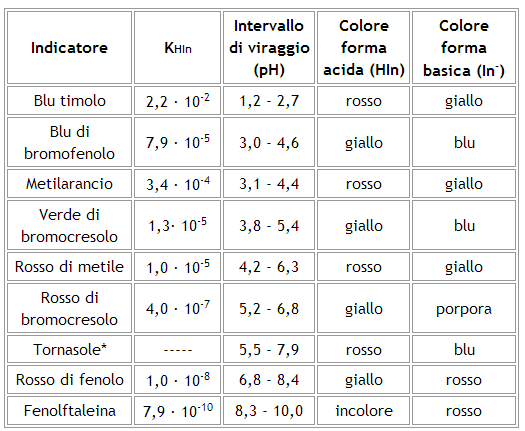
La tabella seguente riporta alcuni indicatori di pH con la relativa costante KHIn, l'intervallo di viraggio e i colori della forma acida (HIn) e della forma basica (In−)
Per approfondimenti si veda:
* Il tornasole (o laccamuffa) è una miscela naturale di parecchi indicatori e pertanto per esso non si può indicare la costante KHIn
Studia con noi