Istidina
Proprietà e caratteristiche dell'istidina
L'istidina è un amminoacido con catena laterale aromatica, essa è presente nelle proteine nella configurazione L.
Il suo nome IUPAC è acido 2(S)-ammino-3-(4-imidazolil)-propanoico, ma è conosciuta anche col nome di L-3-imidazol-4-ilalanina e viene indicata con le sigle His e H.
La sua catena laterale è costituita dal gruppo imidazolico, che le conferisce una pkR (la costante di dissociazione acida del gruppo R) di 6,04, mentre la pk1 (la costante di dissociazione acida del gruppo carbossilico) e la pk2 (la costante di dissociazione acida del gruppo amminico) sono rispettivamente pari a 1,8 e 9,33. La fenilalanina ha un pI (punto isoelettrico) di 7,6.
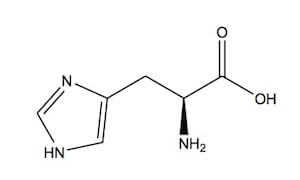
L-istidina.
La formula bruta dell'istidina è C6H9N3O2, pertanto essa ha una massa molare di 155,16 g/mol.
Essa si presenta come un solido cristallino biancastro, ha una solubilità in acqua pari a 38,2 g/L a 20 °C e la sua temperatura di fusione è 272 °C .
Proprietà dell'istidina
L'istidina è un amminoacido essenziale, in quanto essa non può essere prodotta dall'organismo, quindi deve essere assunta con la dieta.
Inizialmente si credeva che fosse un amminoacido essenziale solo per i bambini, ma studi ulteriori hanno stabilito che essa è essenziale anche negli adulti.
Le principali fonti alimentari di questo amminoacido sono: stoccafisso, pancetta e carne di maiale, formaggi (grana, pecorino, gruviera, provolone), vitello, cervo, soia.
L'istidina è necessaria per la crescita e la riparazione tissutale, è importante per il mantenimento della guaina mielinica che protegge le cellule nervose ed è metabolizzata per formare la carnosina, una molecola che previene l'invecchiamento e l'ossidazione, e, soprattutto, il neurotrasmettitore-neurormone istamina che è fondamentale nell'immunità (l'istamina è una molecola che aumenta la risposta infiammatoria dell'organismo, in particolare a livello della pelle e delle membrane mucose), nella secrezione gastrica e nelle funzioni sessuali.
È stato visto che l'istidina aumenta i livelli plasmatici e probabilmente a livello del sistema nervoso centrale di istamina. Senza un adeguato apporto di istidina nella dieta e nelle riserve cellulari, i livelli di istamina non possono essere mantenuti.
Protegge i tessuti contro il danno causato in seguito a esposizione a radiazioni e metalli pesanti.
L'istidina è, infatti, necessaria per sintetizzare le metallotioneine, una famiglia di proteine con alta affinità per i metalli pesanti, in particolare rame, zinco, cadmio e ferro.
Questa importante proprietà permette a tali proteine di regolare e conservare i metalli in modo tale da prevenire reazioni di ossidazione incontrollate.
L'istidina e altre molecole che contengono il nucleo imidazolico hanno proprietà antiossidanti, antinfiammatorie e antisecretorie. La capacità dell'istidina di proteggere il tessuto infiammato è attribuita alla capacità di fungere da scavenger delle specie reattive dell'ossigeno (ROS), generate dalle cellule durante la risposta infiammatoria acuta.
Essa è necessaria all'organismo anche per regolare e usare minerali essenziali presenti in tracce nell'organismo come rame, zinco, ferro, manganese, molibdeno.
Inoltre, l'escrezione di alcuni metalli pesanti come zinco, rame e nichel avviene per mezzo del legame di questi con l'istidina.
L'istidina, oltre a essere il precursore dell'istamina, svolge anche altre funzioni.
Infatti, essa è richiesta anche per la formazione delle cellule ematiche, essendo un amminoacido presente nell'emoglobina, la proteina che ha la funzione di trasportare l'ossigeno alle cellule.
Alcuni problemi del metabolismo dell'istidina portano ad aumentati livelli dell'amminoacido nel sangue, che possono determinare diversi sintomi: ritardo mentale, problemi fisici, instabilità emozionale, tremore, atassia (un problema del sistema nervoso che si manifesta come mancanza di coordinazione dei muscoli volontari) e psicosi.
La carenza di istidina può portare a un peggioramento delle funzioni cognitiva e mnemonica, oltre che ad alti livelli di ferro nel sangue.
Sono stati riscontrati bassi livelli di istidina in individui con ferite croniche, mentre una bassa concentrazione di istidina è tipica di pazienti con artrite reumatoide.
L'istidina, quando è somministrata in quantità terapeutiche, è capace di inibire le citochine e i fattori di crescita coinvolti nel danno cellulare e tissutale.
L'istidina, nella dose di 4.5 grammi al giorno, è stata usata per trattare pazienti con artrite reumatoide.
C'erano evidenze di effetti benefici di tale amminoacido in pazienti con la malattia nella forma più grave e prolungata, basate sulla valutazione in doppio cieco di medici e pazienti.
Pazienti con artrite reumatoide hanno bassi livelli di istidina nel sangue, a causa della rapida rimozione dell'istidina dal circolo sanguigno. Altri pazienti, oltre a quelli con l'artrite, che presentano basse concentrazioni di istidina sono quelli con insufficienza renale cronica.
La concentrazione urinaria di istidina è ridotta in pazienti pediatrici con polmonite, mentre quelli asmatici hanno elevati livelli ematici dell'amminoacido.
La concentrazione plasmatica di istidina è più bassa in caso di infiammazione e stress ossidativo in donne obese.
È stato mostrato che l'utilizzo di integratori di istidina riduce la resistenza all'insulina, l'indice di massa corporea e l'espressione di massa grassa, probabilmente per mezzo del pathway di NF-kB (fattore di trascrizione) negli adipociti.
Ridotte concentrazioni plasmatiche di istamina, associate a scarse quantità di istidina, sono state riscontrate in pazienti con artrite reumatoide e affetti da patologie psichiatriche.
Individui con tossicità da metalli pesanti, inclusi piombo, mercurio e cadmio, quelli che soffrono di allergie stagionali croniche o individui che seguono una dieta con bassi livelli di istidina sono più suscettibili a carenze di riserve di istidina, portando alla possibilità di squilibri che coinvolgono enzimi e minerali.
Biochimica dell'istidina
L'istidina può essere sintetizzata solamente dalle piante e dai microrganismi, ma non dagli animali e dall'uomo.
Come già visto, l'istidina è il precursore dell'istamina.
La reazione di decarbossilazione dell'amminoacido, catalizzata dall'enzima L-istidina decarbossilasi, prevede la perdita di una molecola di anidride carbonica. L'enzima coinvolto in questa reazione richiede vitamina B6 come cofattore.
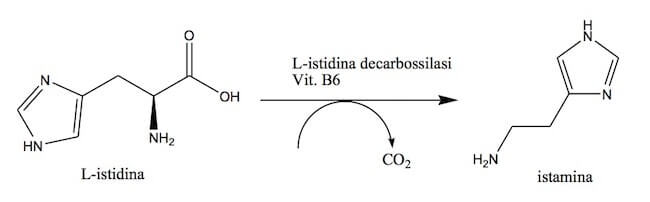
Reazione di biosintesi dell'istamina.
L'istidina è un precursore dell'α-chetoglutarato, una biomolecola di rilievo, poiché prende parte al ciclo di Krebs, una tappa fondamentale per il metabolismo energetico.
Dal momento che l'amminoacido ha 5 atomi di carbonio di fila, esso è un precursore del glutammato, che, a sua volta, è il precursore diretto dell'α-chetoglutarato.
Il processo che porta alla formazione di glutammato a partire dall'istidina (presente nell'organismo in forma ionizzata) è abbastanza complesso; infatti, è necessario l'intervento di 4 enzimi:
- l'istidina ammoniaca liasi, che catalizza la reazione in cui viene eliminato un atomo di azoto sotto forma di ione ammonio;
- l'urocanato idratasi, che elimina una molecola d'acqua;
- l'imidazolone propionasi, che elimina un'ulteriore molecola d'acqua;
- la glutammato formimmino trasferasi, che utilizza il tetraidrofolato in qualità di cofattore e rimuove l'atomo di carbonio in eccesso.
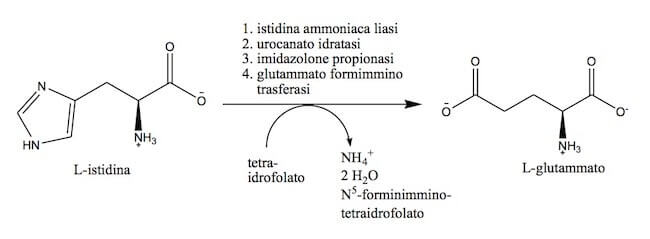
Reazione complessiva di formazione del glutammato a partire dall'istidina.
L'istidina è, insieme alla β-alanina, il costituente della carnosina, un dipeptide importante per il funzionamento di muscoli e cervello.
La reazione di formazione della carnosina è una reazione di condensazione catalizzata dall'enzima carnosina sintasi, che consuma una molecola di ATP; si formano come sottoprodotti quindi AMP e pirofosfato, che viene poi idrolizzato a 2 molecole di fosfato in una reazione catalizzata dalla pirofosfatasi inorganica.
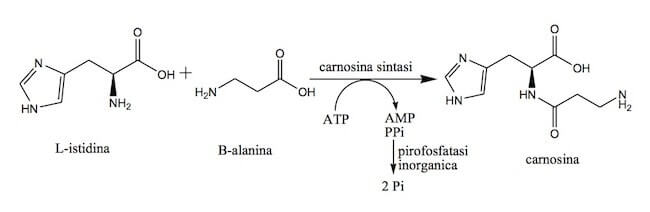
Biosintesi della carnitina.
Durante il processo di traduzione o sintesi proteica, l'amminoacido istidina è codificato dalle triplette di nucleotidi CAT e CAC.
Link correlati:
Proprietà della guanidina
Studia con noi